Farmakologisk behandling
Vårdprogrammet är under uppdatering och beräknas vara helt färdigt i början på juni 2026
Frakturförebyggande åtgärder och behandling
Att förebygga frakturer utgår från de två viktigaste riskfaktorerna – att stärka skelettet och att förhindra fall.
Idag finns effektiva läkemedel för att stärka skelettet medan fysisk träning och belastning av skelettet bidrar till att i första hand bibehålla skelettets egenskaper. Fallprevention är ett vidare begrepp som innefattar flera modaliteter; både att stärka den fysiska förmågan, balans och koordination som att undanröja risker som kan bidra till fall. Dessa risker är både relaterade till person och till den externa miljön och behöver anpassas varje patients förutsättningar
Vilka ska ha läkemedelsbehandling? Beslut om benspecifik behandling ska grundas på en samlad klinisk värdering, baserat både på bentäthetsvärden, uppskattning av frakturrisken, patientens hälsotillstånd, eventuella sekundära orsaker och värdering av nytta vs. risk för biverkningar. Ju högre frakturrisk desto starkare behandlingsindikation.
Ingången för ställningstagande till behandling baseras ofta på hur patienten identifieras: 1) nyligen genomgången fraktur där patienten identifieras via frakturkedjan, 2) tidigare genomgången fraktur där patienten inte identifieras inom en frakturkedja och frakturen kan ligga relativt nära i tid eller för många år sedan eller som vid kotfraktur, uppmärksamma längdminskning eller kronisk ryggsmärta eller 3) inga frakturer och identifieras genom riskfaktorer eller vid andra sjukdomar.
Åldersberoende interventionsgränser
Den sannolikhet som krävs för att behandling ska vara motiverad, den s.k. interventionsgränsen, definieras som sannolikheten för ny fraktur hos en postmenopausal kvinna med tidigare fraktur vid en given ålder. Även om frakturrisken inom 10-år (enligt FRAX) hos en kvinna med osteoporos i 55-årsåldern är mycket lägre än för en kvinna med samma tillstånd i 70-års ålder, är livstidrisken för fraktur hos den yngre kvinnan mycket hög. Risken för höftfraktur för kvinnor med osteoporos och yngre än 70 år överstiger 27% under en 25-årsperiod (45). Utan intervention förväntas bentätheten successivt minska med ökande ålder vilket bidrar till den gradvisa ökningen av frakturrisken. Det är därför högst rimligt att hos patienter med låg bentäthet förbättra bentätheten och därmed minska frakturrisken på lång sikt. Val av behandling avgörs av ålder, bentäthet och frakturrisk. Eftersom frakturrisken påverkas av åldern, sätts den åldersberoende interventionsgränsen lägre hos yngre än hos äldre kvinnor för att långsiktigt minska deras frakturrisk (Figur 1 och Tabell 1). Val av behandling och behandlingsintervall beror på hur nedsatt bentäthen är och hur hög frakturrisken är (se avsnitt om Farmakologisk behandling).
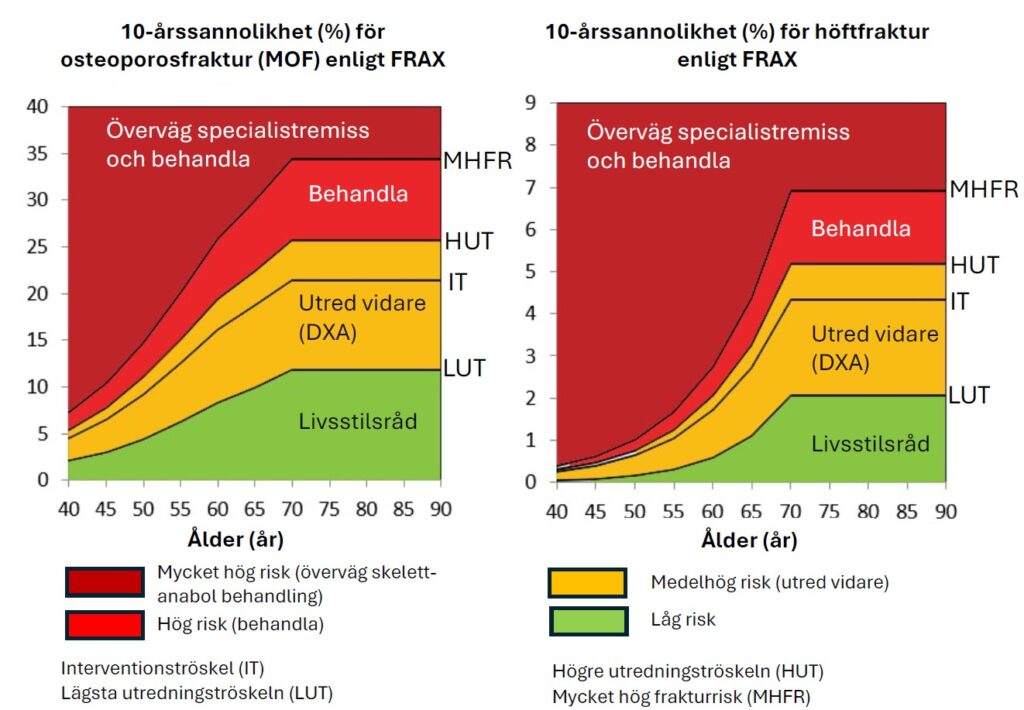
Osteoporosfraktur (MOF) – gränser för 10-årssannolikheter (%)
| Ålder | IT | LUT | HUT | MHFR |
| 40 | 4,5 | 2,1 | 5,4 | 7,2 |
| 45 | 6,5 | 3,0 | 7,8 | 10,4 |
| 50 | 9,2 | 4,4 | 11,0 | 14,7 |
| 55 | 12,6 | 6,3 | 15,1 | 20,1 |
| 60 | 16,1 | 8,3 | 19,3 | 25,8 |
| 65 | 18,7 | 9,9 | 22,5 | 29,9 |
| 70 | 21,5 | 11,8 | 25,8 | 34,4 |
| 75 | 21,5 | 11,8 | 25,8 | 34,4 |
| 80 | 21,5 | 11,8 | 25,8 | 34,4 |
| 85 | 21,5 | 11,8 | 25,8 | 34,4 |
| 90 | 21,5 | 11,8 | 25,8 | 34,4 |
Höftfraktur – gränser för 10-årssannolikheter (%)
| Ålder | IT | LUT | HUT | MHFR |
| 40 | 0,2 | 0,0 | 0,3 | 0,4 |
| 45 | 0,4 | 0,1 | 0,5 | 0,6 |
| 50 | 0,6 | 0,2 | 0,8 | 1,0 |
| 55 | 1,0 | 0,3 | 1,3 | 1,7 |
| 60 | 1,7 | 0,6 | 2,1 | 2,7 |
| 65 | 2,7 | 1,1 | 3,3 | 4,4 |
| 70 | 4,3 | 2,1 | 5,2 | 6,9 |
| 75 | 4,3 | 2,1 | 5,2 | 6,9 |
| 80 | 4,3 | 2,1 | 5,2 | 6,9 |
| 85 | 4,3 | 2,1 | 5,2 | 6,9 |
| 90 | 4,3 | 2,1 | 5,2 | 6,9 |
Figur 1 och tabell 1 a och 1 b. Åldersberoende 10-årssannolikheter (%) och gränser för utredning och behandling för osteoporosfraktur (vänster) och höftfraktur (höger) enligt FRAX för Sverige. IT=Interventionströskeln, LUT=Lägsta utredningströskeln, HUT=Högre utredningströskeln. MHFR=Mycket hög frakturrisk. Illustrationer som anpassats från (1).
Hos yngre postmenopausala kvinnor, som slutat menstruera nyligen (de senaste 10 åren), kan man under vissa villkor överväga hormonersättningsbehandling, alternativt infusion zoledronsyra med varierande förlängt behandlingsintervall (se efterföljande stycke).
En första riskbedömning kan göras utifrån kliniska riskfaktorer, ålder och kön, enligt Figur 1. För personer med risk som överstiger den lägsta interventionströskeln för utredning med DXA bör remitteras för bentäthetsmätning, för att 1) ge vägledning till om behandling ska ges och 2) för att avgöra typ av behandling, då skelettanabol behandling bör övervägas vid mycket hög frakturrisk (44) eller mycket låg bentäthet. Med hjälp av bentäthetsvärdet kan en ny FRAX-bedömning utföras där bentäthet i lårbenshalsen tas med vilket ger en säkrare frakturriskbedömning (Figur 2).
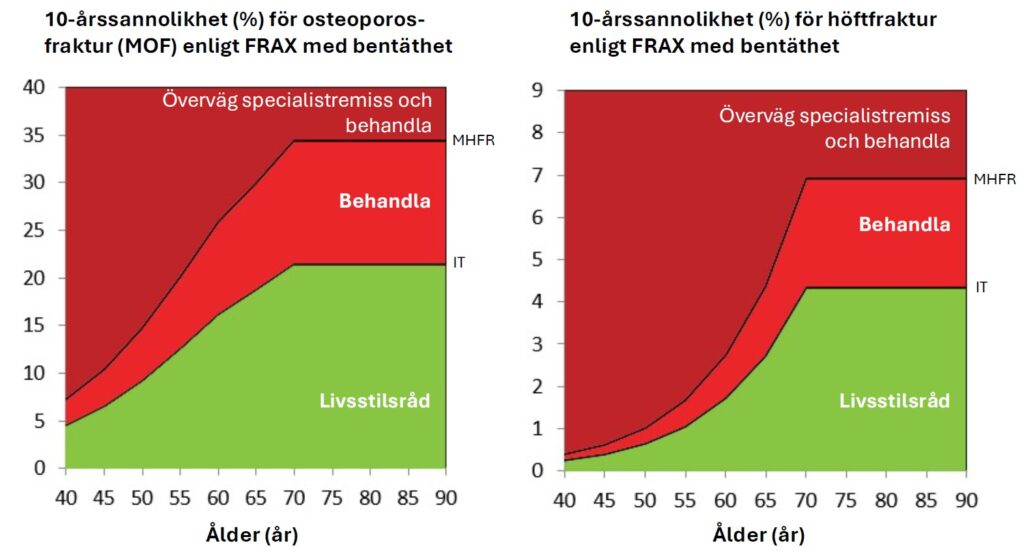
Figur 2 A och B. Rekommendation om behandling utifrån frakturrisk. Frakturrisk (MOF – A och höftfraktur – B) och behandlingsförslag illustreras med färger, där grönt indikerar att enbart livsstilsråd bör ges, rött att indikation för läkemedelsbehandling föreligger och mörkrött att sekventiell behandling (skelettanabola följt av antiresorptiv) bör övervägas. Från och med 70 års-ålder används fasta interventionsgränser (IG) på 21,5% för MOF och 4,3% för höftfraktur. Notera dock att även andra kriterier gäller för övervägande av skelettanabol behandling. IT=Interventionströskeln, MHFR=Mycket hög frakturrisk. Illustrationer som anpassats från (1).
Behandlingsindikation
Behandling med osteoporosläkemedel bör alltid övervägas till:
- Patienter med nyligen genomgången eller tidigare fraktur i höft eller kota, oavsett bentäthet om det inte finns kontraindikationer
- Patient med annan nyligen eller tidigare genomgången osteoporosrelaterad fraktur och hög frakturrisk, över den åldersspecifika interventionsgränsen för osteoporosfraktur eller höftfraktur enligt FRAX, samt låg bentäthet (≤-1 i T-score)
- Patienter med låg bentäthet (≤-2.5 i T-score) och hög frakturrisk, över interventionsgränsen enligt FRAX för osteoporosfraktur eller höftfraktur.
- Patienter med peroral kortisonbehandling (mer än motsvarande 5 mg prednisolon dagligen och förväntad behandlingstid överstigande 3 mån). Se separat avsnitt om benspecifik behandling vid p.o. kortison (Faktaruta 5)
Medicinsk behandling bör även övervägas till kvinnor i menopausal ålder eller tidigt postmenopausala kvinnor med låg bentäthet, osteoporos eller osteopeni, och riskfaktorer som indikerar ökad risk att utveckla osteoporos, t.ex. med ärftlighet, men som inte har en 10-årsrisk som överstiger interventionströskeln. I denna grupp är ofta frakturrisken låg på kort sikt tack vare den låga åldern, men då benförlusten är accelererad de första åren efter menopausen och behandlingar som förebygger osteoporosutveckling är tillgängliga kan man överväga
- Systemisk menopausal hormonell behandling (MHT) (46). Vid samtidiga klimakteriella symptom och ålder <60 år (behandlingen bör lämpligen fortsätta med antiresorptiv behandling efter MHT, med ny riskbedömning och DXA innan byte) eller
- zoledronsyrabehandling (se under avsnittet Zoledronsyrabehandling för att förebygga osteoporosutveckling) med varierande intervall, årligen vid osteoporos, eller vart annat till vart femte år vid låg bentäthet
då dessa behandlingar förebygger frakturer genom att förhindra den åldersberoende benförlusten och därmed förhindrar osteoporosutveckling hos en betydande andel (47, 48).
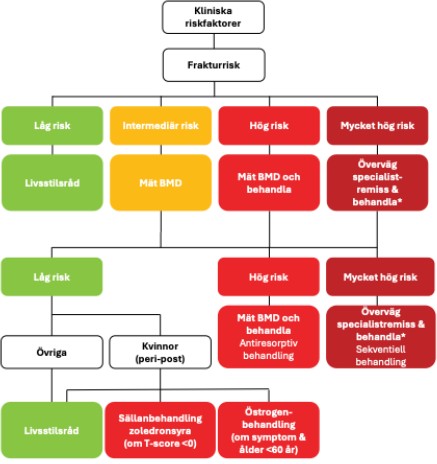
Figur 3. Sammanfattning av riskbedömning och handläggning. Indikationen för behandling och behandlingsval bör alltid utgå från den samlade riskvärderingen och patientens totala hälsosituation. Illustration som anpassats från (1). *Behandling med skelettanabolt läkemedel först, dvs. ge inte antiresorptivt läkemedel i avvaktan på specialistbedömning.
Läkemedelsbehandling
Systemisk hormonell behandling (MHT)
MHT omfattar flera olika preparat med antingen östrogen enbart eller en kombination av östrogen och gestagen (inklusive syntetiska gestagener eller kroppseget progesteron). En del av dessa är godkända som andrahandspreparat, för att förebygga osteoporos hos postmenopausala kvinnor som har en ökad risk för osteoporosfrakturer.
En kombination av konjugerade hästöstrogener (0,625 mg dagligen) med eller utan medroxyprogesteronacetat (2,5 mg dagligen) har visat sig minska risken för kot-, icke-vertebrala och höftfrakturer hos postmenopausala kvinnor, även hos dem som inte valdes ut baserat på låg bentäthet eller hög frakturrisk (49, 50). Både per orala (Activelle, Femanest) och transdermala (Estrogel) östrogenpreparat finns tillgängliga i Sverige för förbyggande av osteoporos hos postmenopausala kvinnor, om de har kontraindikationer mot osteoporosläkemedel (www.fass.se).
Biverkningsrisker
Risken för venös blodpropp (VTE) ökar vid användning av orala östrogenbaserade HRT-preparat jämfört med bakgrundsbefolkningen, men denna riskökning ses inte med transdermala MHT-preparat i standarddosering.
MHT ökar inte risken för hjärt-kärlsjukdom när behandlingen inleds hos kvinnor under 60 år. Om den påbörjas inom tio år efter menopaus verkar den snarare minska risken för hjärt-kärlsjukdom (51).
Vissa MHT-preparat, framför allt de som innehåller syntetiska gestagener, är kopplade till en något ökad risk för bröstcancer. Denna risk är dock mindre än den som följer av negativa livsstilsfaktorer såsom låg fysisk aktivitet, övervikt och hög alkoholkonsumtion.
För kvinnor med låg grundrisk för bröstcancer (vilket gäller för de flesta), överväger fördelarna med MHT när det används i upp till fem år för symtomlindring enbart klart de eventuella riskerna – även utan att beakta dess positiva effekter på skelettet. I nyligen (2025) publicerade nationella riktlinjer från Socialstyrelsen om klimakteriebesvär ges hög prioritet (3 av 10) för systemisk hormonell behandling (MHT) för kvinnor i menopausålder med förhöjd risk för osteoporos (46).
Basbehandling med kalcium och vitamin D
Benspecifika läkemedel ska i de allra flesta fall kombineras med tillskott av kalcium och vitamin D. Kalcium och vitamin D (kolekalciferol) ges som tillägg till annan benspecifik läkemedelsbehandling om tillräckligt intag (adekvat dagligt intag av kalcium: 800 mg och för D-vitamin: 800 IE) inte kan säkerställas. Eftersom den frakturförebyggande effekten är otillräcklig/tveksam används kalcium och vitamin D ej enskilt eller i kombination, som monoterapi vid osteoporos.
Tips: Påbörja behandling med kalcium-Vitamin D 500 mg + 400-800E /dag 1-2 veckor innan benspecifik behandling. Det underlättar i att bedöma om eventuella gastrointestinala biverkningar är relaterade till kalcium snarare än det specifika läkemedlet. Kalcium tas upp bäst om tabletter tas med måltid.
Efter avslutad behandling med bisfosfonater kan man fortsätta med kalcium och vitamin D om konstaterad brist på kalcium och D-vitamin eller om tillräckligt intag inte kan säkerställas vid kostanamnes.
Benspecifika läkemedel
Benspecifika läkemedel definieras som antingen antiresorptiva (hämmar osteoklasternas aktivitet) eller skelettanabola (stimulerar osteoblaster till ny benbildning). Läkemedlens effekt i form av riskreduktion för frakturer är väl dokumenterad (44). Samtliga läkemedel nedan är godkända för behandling av både kvinnor och män med ökad risk för fraktur (med undantag för romosozumab). Val av läkemedel avgörs av bedömning av patientens risk och totala hälsosituation samt risk för eventuella biverkningar. Följsamheten är mycket bättre vid parenteral än vid per oral osteoporosbehandling.
Antiresorptiva läkemedel – bisfosfonater och denosumab
Bisfosfonater
Bisfosfonater är förstahandsbehandling i de flesta fall enligt nationella och internationella rekommendationer. I stora, randomiserade placebokontrollerade studier minskar både alendronat och zoledronsyra (de vanligen använda bisfosfonaterna) risken för kot-, höftfraktur och andra frakturer jämfört med placebo, hos postmenopausala kvinnor med låg bentäthet. Riskminskningen har varit cirka 50%-70% för kotfrakturer, cirka 40% för höftfrakturer och cirka 20% för icke-kotfrakturer i 3-åriga studier på högriskpatienter (52) (53) (54).
Behandling med alendronat och zoledronsyra förutsätter att kreatininclearence är 35 ml/min eller högre varför kreatinin måste kontrolleras inom 3 månader före behandling. Även kalcium, 25-OH-D-vitamin och PTH bör kontrolleras, eftersom antiresorptiv behandling är olämplig vid obehandlad hypokalcemi och D-vitaminbrist skall korrigeras före behandling.
Zoledronsyra har bättre följsamhet, fördelaktigt administrationssätt, vilket gör att läkemedlet rekommenderas som förstahandsval (55).
Zoledronsyra 5 mg iv infusion 1 ggr/år
Dosering: 5 mg iv infusion 1 ggr/år vid låg bentäthet.
Initialt behandlas patienten vanligen under 3 år. Behandlingstiden kan förlängas upp till 6 år för patienter med kvarvarande hög frakturrisk (samma kriterier som för förlängd behandling med alendronat dvs mer än en kotfraktur eller osteoporotiskt mätvärde i höft).
Zoledronsyra har längst retentionstid i benvävnaden av bisfosfonaterna. Efter utsättning avtar även här effekten och man bör räkna med att återinsätta zoledronsyra senast efter cirka 6 års uppehåll. DXA-mätning vart 3:e år efter utsättning rekommenderas om det påverkar fortsatt handläggning.
Zoledronsyra, intravenös bisfosfonatbehandling. Infusion ges i öppenvård under minst 15 minuter, följt av 10 minuters vila innan patienten kan lämna mottagningen. Då patienten inte får vara dehydrerad ska hen dricka 1-2 glas vatten före och efter infusionen. Intag av paracetamol 1g 2-4 gånger rekommenderas under infusionsdagen, för att minska risken för influensaliknande biverkningar.
Den förväntade effekten av zoledronsyra 5mg årligen i 3 år uppgår till drygt 4% (drygt 1/3 T-score) förbättring av bentäthet i total höft och ca 8% i ländryggen. Effekten blir inte bättre i total höft efter 6 års behandling, men ökar med ca 2% ytterligare i ländryggen (56).
Zoledronsyrabehandling för att förebygga osteoporosutveckling
Dosering: 5 mg iv infusion 1 ggr/18-60 månader vid låg bentäthet.
Hos yngre postmenopausala kvinnor över 50 år kan man överväga sällanbehandling med zoledronsyra, även i primärpreventivt syfte vid påvisad osteopeni eller bentäthet T-score <0, vid förekomst av riskfaktorer, så som t.ex. ärftlighet för osteoporos. Jämfört med placebo kan zoledronsyra (5 mg iv.) var 18:e månad hos postmenopausala kvinnor med osteopeni förbättra bentätheten och minska frakturrisken under en 6-årsperiod (57). Dessutom har behandling med zoledronsyra (5 mg iv.) 1 gång vart 5:e år under 10 år visats kunna förbättra bentätheten och minska frakturrisken hos tidigt postmenopausala kvinnor med normal till låg (osteopeni) bentäthet, jämfört med placebo (48). Således kan behandlingen övervägas med 18-60 månaders intervall, beroende på bentäthet och frakturrisk. Det kortare intervallet bör då tillämpas vid lägre bentäthet och högre frakturrisk, medan det längre intervallet kan vara lämpligt vid lägre frakturrisk och högre bentäthet i denna patientgrupp.
Alendronat, 70 mg tablett 1 ggr/ vecka
Dosering: 70 mg tablett 1 ggr/ vecka.
Initialt behandlas patienten under 3-5 år, vanligen 5 år. Därefter tar man ställning till fortsatt behandling baserat på patientens riskprofil och bentäthet.
Om patienten haft mer än en kotfraktur eller har kvarstående osteoporos i höft (T-score < -2,5) fortsätter man vanligen behandlingen i upp till maximalt 10 år.
Efter utsatt alendronat kan man göra ny DXA efter 3 år och därefter 2 år om återinsättning kan bli aktuell. Vid signifikant sjunkande bentäthet återinsätts alendronat under cirka 3 år. Alendronat bör återinsättas efter 5 år oavsett om bentätheten sjunkit och då under 3 års tid och därefter upprepas proceduren.
Alendronat veckotablett 70 mg skall tas på fastande mage med ett stort glas vatten, minst 30 minuter före frukost. Patienten får inte ligga förrän efter frukost. Kalcium ska inte tas i nära anknytning till perorala bisfosfonater, enklast för patienter är därför att ta kalcium och D-vitamin på kvällen.
Den förväntade effekten av alendronat 5 år uppgår till drygt 2.4% (drygt 1/5 T-score) förbättring av bentäthet i total höft och drygt 8% i ländryggen. Effekten blir inte bättre i total höft efter 10 års behandling, men ökar med knappt 7% ytterligare i ländryggen (61).
Risedronat, 35 mg tablett 1 ggr/ vecka
Dosering: 35 mg tablett 1 ggr/ vecka.
Risedronat är en bisfosfonat som ibland används vid biverkningar av alendronat. Såväl effekt som biverkningsprofil liknar de av alendronat och veckotabletten tas på samma sätt. Behandlingstiden rekommenderas på samma sätt. Man bör dock beakta att retentionstiden i skelettet är något kortare än för alendronat och DXA-mätning bör utföras vartannat år efter utsättning. Man kan för risedronat förvänta sig att behöva återinsätta läkemedlet inom 3-4 år efter utsättning.
Denosumab 60 mg subkutan injektion var 6:e månad
Dosering: 60 mg subkutan injektion var 6:e månad.
Denosumab är en human antikropp riktad mot RANK-ligand och är ett alternativ till bisfosfonater vid nedsatt njurfunktion eller där bisfosfonater inte tolererats eller av annan anledning inte bedöms lämpliga. Denosumab minskar hos postmenopausala kvinnor med osteoporos risken för kotfraktur med cirka 70%, för höftfraktur med cirka 40% och övriga frakturer cirka 20% jämfört med placebo (58).
Före första injektionen skall kalcium och kreatinin kontrolleras. Enligt FASS skall kalcium kontrolleras före varje injektion, men på en del kliniker kontrolleras kalcium en gång per år om kalcium varit stabilt efter de första injektionerna.
Denosumab skall inte utan noggrant övervägande utsättas utan behandlingen bör fortgå kontinuerligt. Effekten av denosumab avtar snabbt cirka 6 månader efter den senaste injektionen, och bentätheten förväntas cirka 18 månader efter den senaste injektionen ha återgått till den nivå man hade före insättning, även om patienten behandlats i flera år. Detta gör att den frakturreducerande effekten snabbt avtar efter utsättning. Om man trots detta behöver/önskar avsluta behandling med denosumab så skall den efterföljas av en behandlingsperiod med bisfosfonater (förutsatt att patienten tål detta med avseende på njurfunktion).
Denosumab ger större förbättringar i bentäthet i höften och i ländryggen än alendronat och zoledronsyra (59). Till skillnad från bisfosfonatbehandling avtar inte ökningarna med behandlingstiden utan fortsätter i minst 10 år. Efter 10 års behandling har bentätheten ökat över 9% i total höft och 22% i ländryggen (60).
Behandling med denosumab kan ge förhöjd risk för hypokalcemi. Särskild försiktighet bör iakttas hos patienter med uttalat nedsatt njurfunktion. Kontroll av kalcium och PTH skall vid njurinsufficiens alltid göras före första dosen och såväl ett lågt serumkalcium som ett förhöjt PTH (sekundär hyperparatyroidism) kan indikera ökad risk för hypokalcemi. Risken för hypokalcemi är störst vid första injektionen men S-kalcium skall kontrolleras före varje dos denosumab vid njurinsufficiens.
Hos patienter med uttalat nedsatt njurfunktion (GFR<30ml/min) och framför allt vid högt PTH, är risken för hypokalcemi särskilt stor. Då bör injektionen föregås av ökat intag av kalcium under ett par veckors tid, eventuellt aktivt vitamin D samt kontroller av kalcium före och tämligen snart efter injektionen (4-7 dagar efter injektion plus 4-7 dagar senare). Före första injektionen bör man vid osäkerhet rådgöra med njurmedicinsk specialist, eller läkare med vana att behandla patienter med uttalat nedsatt njurfunktion med denosumab.
Skelettanabola läkemedel och sekventiell behandling
De anabola läkemedlen teriparatid och romosozumab har i randomiserade studier visats mer effektiva än bisfosfonater för patienter med mycket hög frakturrisk som haft en eller flera kotfrakturer (44) (62) (63). De ger en större ökning i bentäthet och minskar frakturrisken signifikant jämfört med bisfosfonater. Effekten av de anabola läkemedlen på bentäthet blir bättre om behandlingssekvensen inleds med anabol behandling än om antiresorptiv behandling ges först (64, 65). Därför är det viktigt att de övervägs tidigt för selekterade patienter med mycket hög frakturrisk. För att bibehålla den minskade frakturrisken och den ökade benmassan är det dessutom viktigt att man vid behandlingsslut fortsätter med antiresorptiva läkemedel, s.k. sekventiell behandling vilket är praxis. Benuppbyggande läkemedel är mer kostsamma än antiresorptiva läkemedel.
För patienter med mycket hög frakturrisk och låg bentäthet bör behandlingen individualiseras och sekventiell behandling kan övervägas. Det kan till exempel vara patienter med en eller flera kliniska kotfrakturer samt kotfrakturer i samband med kronisk kortisonbehandling. Även till patienter med andra frakturer, mycket hög risk och låg bentäthet kan sekventiell behandling övervägas. Skelettanabola läkemedel (teriparatid eller romosozumab) bör insättas av specialister väl förtrogna med handläggning av osteoporospatienter.
Vilka bör övervägas för skelettanabol behandling?
Sammanfattningsvis, remiss till osteoporosspecialist och övervägande av skelettanabola läkemedel bör göras vid misstanke om mycket hög frakturrisk. Exempel på tillstånd:
- Förekomst av en klinisk kotfraktur nyligen (senaste 2 åren) efter lågenergitrauma
- Förekomst av 2 kotfrakturer, oavsett när de inträffade
- Klinisk kotfraktur och pågående per oral kortisonbehandling (minst 5 mg prednisolon dagligen under minst 3 månader)
- Mycket hög frakturrisk (t.ex. FRAX eller annan riskvärdering) i kombination med låg bentäthet (se Figur 2)
- Uttalat låg bentäthet (< -3,0 i T-score i ländrygg eller < -2.8 i totalhöft)
Teriparatid
Dosering: 20 μg daglig subkutan injektion.
Teriparatid är ett fragment av humant parathormon, innehåller den aktiva delen (1-34) och verkar direkt på osteoblasterna. Behandling med teriparatid medförde en signifikant lägre risk för kotfraktur och klinisk fraktur jämfört med risedronat i en studie av postmenopausala kvinnor med hög frakturrisk och kotfraktur (VERO) (63). I VERO-studien randomiserades 1360 kvinnor med en svår eller två måttliga kotfrakturer och låg bentäthet (<-1.5 SD i T-score) till teriparatid eller risedronat under 24 månader. Studien visade betydligt lägre incidens av nya kotfrakturer (56% lägre relativ risk) och 52% lägre risk för klinisk fraktur i teriparatidgruppen oavsett om man var behandlingsnaiv eller hade behandlats med bisfosfonater före studiens start.
Långtidseffekten på bentäthet blir större om teriparatid ges före antiresorptiv behandling (s.k sekventiell behandling) jämfört med att börja med enbart antiresorptiv behandling (54). Teriparatid är bland annat kontraindicerat vid tumörer i skelettet och efter strålbehandling.
Teriparatid ges från 18 till maximalt 24 månader. Viktigt att vid utsättning övergå till antiresorptivt läkemedel för att bibehålla effekten av behandlingen och frakturskyddet, då den anabola effekten avtar snabbt efter avslutad behandling
Teriparatid finns nu tillgängligt även i form av biosimilarer och generika, vilket påverkar prisbilden gynnsamt.
Romosozumab
Dosering: 210 mg (två subkutana injektioner på 105 mg vardera) en gång per månad.
Romosozumab är en humaniserad monoklonal antikropp som hämmar sklerostin, vilket medför ökad aktivering av osteoblasteroch hämning av osteoklaster.
Behandling med romosozumab medförde en signifikant lägre risk för fraktur jämfört med alendronat i en studie av postmenopausala kvinnor med osteoporos och kotfraktur eller höftfraktur (62). I ARCH-studien randomiserades 4093 postmenopausala kvinnor med kotfraktur och låg bentäthet till romosozumab eller alendronat i 12 månader, och därefter fick alla deltagare alendronat. Kvinnor som fick romosozumab ökade betydligt mer i bentäthet och hade lägre incidens av nya kotfrakturer och höftfrakturer (50 % lägre relativ risk för kotfraktur och 38% lägre risk för höftfraktur) än kvinnor som enbart fick alendronat.
Romosozumab ges i 12 månader. Romosozumab bör ges som första behandling i den sekventiella behandlingen, eftersom effekten på bentätheten blir bättre med den sekvensen än om behandlingen ges efter en antiresorptiv behandling (64). Viktigt att vid utsättning övergå till antiresorptivt läkemedel för att bibehålla effekten av behandlingen och frakturskyddet, då den anabola effekten avtar snabbt efter avslutad behandling. Romosozumab är kontraindicerat hos patienter med tidigare hjärtinfarkt eller stroke.
Läkemedelsinsättning och behandlingskontroll
Kontrollera följsamhet efter 2-3 månaders behandling med p.o. bisfosfonat (kan med fördel göras per telefon / digitalt).
Om behandlingen föregåtts av DXA-mätning kan bentätheten följas upp beroende på behandlingsplanen, i regel efter 2-3 år men kan t ex utsträckas till 5 år och inför ställningstagande om uppehåll om patienten tolererar behandlingen och har god följsamhet. Hos en del patienter, särskilt de allra äldsta och de som startar behandling med densumab tillsvidare, där behandlingsalternativ saknas, behöver man inte alltid göra en uppföljande DXA-mätning.
Vid behandling med teriparatid utförs DXA-mätningen lämpligen då behandlingen avslutas, dvs vanligen efter 24 månader. Denna behandlingskontroll utgör utgångspunkt för inledning av antiresorptivt läkemedel.
Vid behandling med romosozumab utförs DXA-mätning lämpligen då behandlingen avslutas, dvs efter 12 månader. Denna behandlingskontroll utgör utgångspunkt för inledning av antiresorptivt läkemedel.
Förändring av bentäthet i total höft är den bästa surrogatmarkören för behandlingseffekt. Ju mer bentätheten ökar i total höft, desto mer minskar frakturrisken. Bentäthetsförändring i total höft har visats förklara 73% av variationen i risk för kotfraktur. Därför godkändes måttet i december 2025 som ett acceptabelt surrogatmått för frakturer av Food and Drug Administration i USA för användning i kommande läkemedelsstudier för osteoporospreparat (66, 67). Därmed kan nu nya osteoporosläkemedel godkännas i USA baserat på ökad bentäthet i total höft utan att större studier med fraktur som primärt utfallsmått är nödvändiga.
Vid signifikant sjunkande bentäthet, en nytillkommen kotfraktur eller 2 nytillkomna andra frakturer bör följsamheten kontrolleras (vid p.o och s.c behandling) och terapibyte övervägas. Eventuella orsaker och ytterligare utredning bör övervägas för att utesluta nytillkommen underliggande sjukdom. Om behandlingen bedöms vara framgångsrik behöver bentätheten inte kontrolleras förrän efter ytterligare ca 3 år eller när behandlingen avslutas.
Behandlingssvikt
Behandlingssvikt defineras av förekomst av minst 2 nya frakturer eller av signifikant (utöver LSC) minskad bentäthet under pågående behandling (68). Generellt bör man då överväga att
- Ersätta en svagare antiresorptiv behandling med en starkare
- Byta ett p.o. läkemedel till ett parenteralt
- Byta en stark antiresorptiv behandling till en skelettanabolbehandling (se nedan stycke)
Rekommenderad behandlingssekvens och behandlingsbyte
Effekten av skelettanabola läkemedel är reducerad, med mindre ökningar i bentäthet, om patienten tidigare har behandlats med bisfosfonater eller denosumab, särskilt efter långtidsbehandling. Skelettanabol behandling bör därför, när sådan är indicerad, ges initialt innan antiresorptiv behandling påbörjas. Det är således av central betydelse att redan vid behandlingsstart ta ställning till vilket terapival som är mest lämpligt utifrån osteoporosens svårighetsgrad och patientens frakturrisk.
Eftersom bentätheten successivt minskar efter avslutad skelettanabol behandling bör denna alltid följas av antiresorptiv behandling i syfte att konsolidera och långsiktigt bibehålla samt ytterligare förbättra den uppnådda bentäthetsökningen.
Vid otillräcklig effekt av antiresorptiv behandling kan byte övervägas antingen till en mer potent antiresorptiv behandling (t.ex. från zoledronsyra till denosumab) eller till skelettanabol behandling (t.ex. från zoledronsyra till teriparatid eller romosozumab).
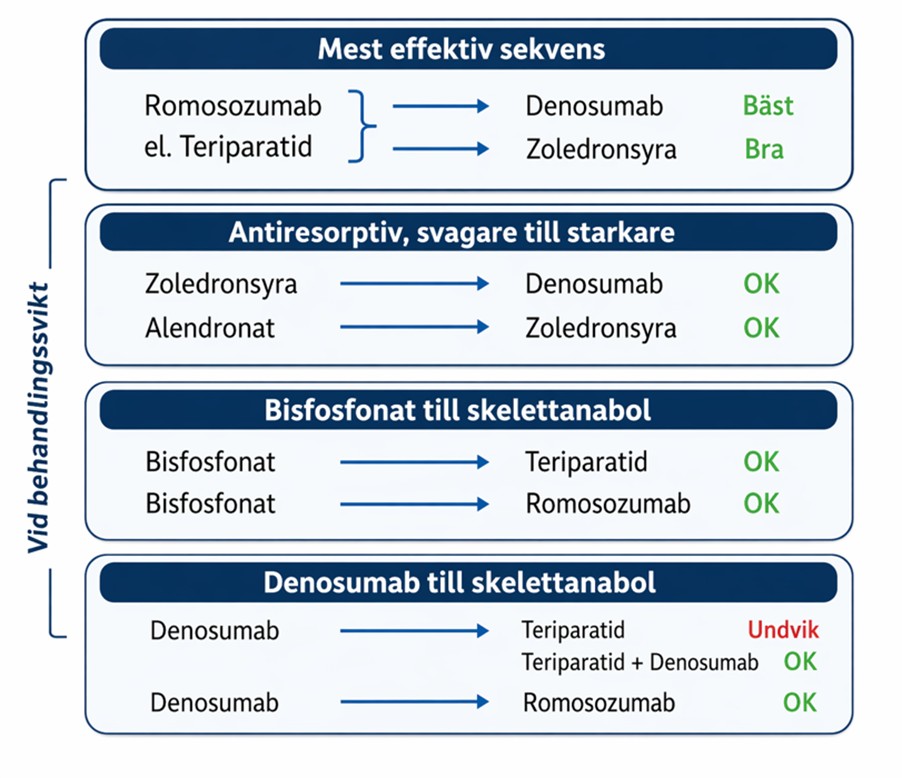
Vid utsättning av denosumab måste dock den kraftiga rebound-ökningen av benomsättningen särskilt beaktas. Byte från denosumab till teriparatid bör undvikas, eftersom teriparatid ytterligare stimulerar benomsättningen och kan leda till minskad bentäthet i detta sammanhang. Om behandling med denosumab ska avslutas och skelettanabol terapi bedöms indicerad, bör byte i stället ske till romosozumab, som förutom sin skelettanabola effekt även har antiresorptiva egenskaper. Detta möjliggör i regel fortsatt ökning av bentätheten vid behandlingsskifte. Om stark indikation för skelettanabol behandling och kontraindikationer föreligger för romosozumab, kan man fortsätta behandlingen med denosumab och lägga till teriparatid under 18-24 månader (Figur 4).
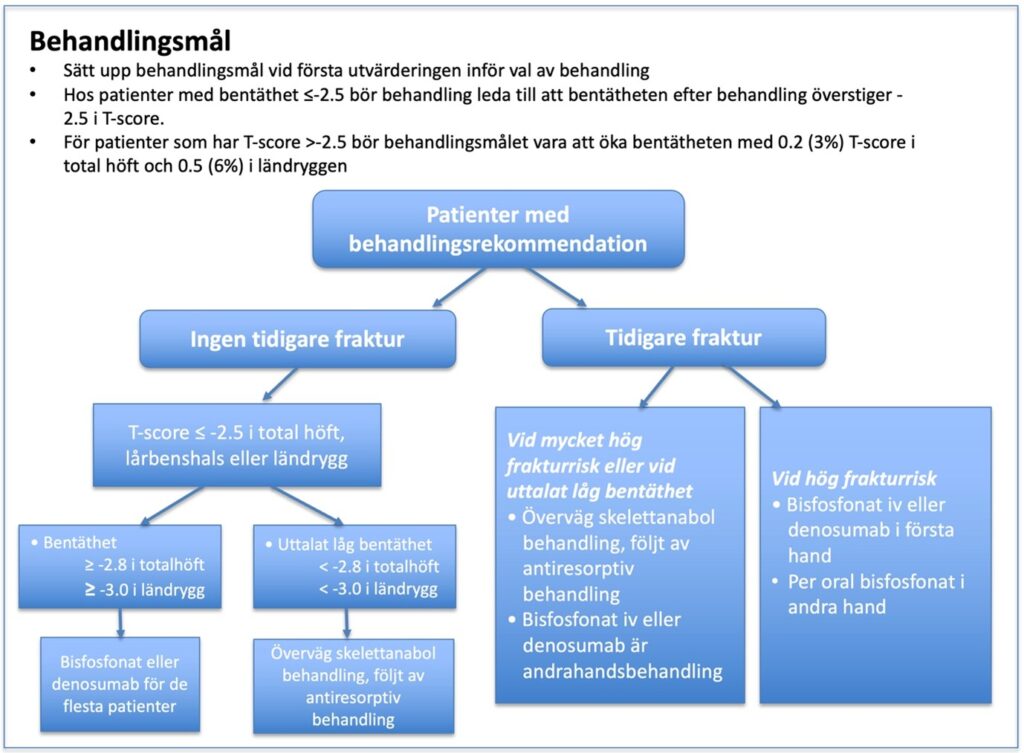
Målstyrd behandling ”Treat-to-Target”
Målet med den farmakologiska behandlingen är att uppnå tillräckligt minskning av frakturrisken tillräckligt snabbt. Ett mål bör bestämmas vid första besöket och målet bör styra val av behandling. Eftersom den mest optimala behandlingssekvensen är skelettanabol följt av antiresorptiv behandling är det viktigt att behandlingsmålet bestäms direkt, innan patienten fått antiresorptiv behandling, eftersom denna – speciellt vid långtidsbehandling – försämrar effekten hos skelettanabola läkemedel (69) (64).
Hos patienter med bentäthet <-2.5 och fraktur bör behandling eftersträva att bentätheten efter behandling åtminstone överstiger -2.5 i T-score i total höft. För patienter som har T-score >-2.5 bör behandlingsmålet vara att öka bentätheten med minst 0.2 (3%) T-score i total höft och 0.5 (6%) i ländryggen (70). Frakturrisken minskar successivt med behandling som ökar bentätheten till nivåer omkring -2 till -1.5 i T-score i total höft (71). Baserat på känd effekt av antiresorptiv behandling på bentäthet bör man även överväga skelettanabol behandling då bentätheten är uttalat låg, dvs. inte bara vid mycket hög frakturrisk. Se flödesschma för råd om målstyrd behandling (Figur 5).
Läkemedelsbiverkningar
Biverkningar vid antiresorptiv behandling
Mag- och tarmbesvär rapporteras inte sällan vid peroral bisfosfonatbehandling, något oftare i samband med alendronat. Led- och muskelsmärta förekommer hos cirka 2-3 % av patienter under behandling med perorala bisfosfonater. Vid intravenös behandling med zoledronsyra är det vanligt med feber, muskel-, led- och huvudvärk samt influensaliknande symptom under 1-2 dygn efter infusionen. Risken för biverkningar avtar med infusionstillfälle (45% vid 1:a dosen till 10% vid 3:e dosen) och om profylax med analgetika används (19% till 10%, 1:a respektive 3:e dos).
I registreringsstudien för denosumab (FREEDOM), rapporterades en ökad risk för hudinfektion som ledde till sjukhusinläggning (0,4% vs. 0,1% i placebogruppen), samt för eksem, men dessa biverkningar har inte observerats i efterföljande stora läkemedelsstudier (72). Risk för hypokalcemi skall beaktas för vissa grupper ffa hos patienter med njurinsufficiens och malabsorption, se ovan.
Biverkningar vid skelettanabol behandling
Generellt, vid behandling med teriparatid är eventuella biverkningarna milda och övergående. Vanliga biverkningar inkluderar illamående, yrsel (3-9%), ortostatisk hypotension, benkramper (ca 3%) och hyperkalcemi, vanligtvis mild. Observera att om man kontrollerar kalcium, så bör patienten provtagningsdagen ta teriparatid och eventuell kalciumtablett efter provtagningen. Osteosarkom har observerats hos råttor, men ingen sådan ökad risk har påvisats hos människor som behandlats med teriparatid. Teriparatid är kontraindicerat hos patienter med skelettmetastasering, osteosarkom eller om skelettet strålbehandlats.
Vid behandling med romosozumab är eventuella biverkningarna milda och övergående. En vanlig biverkan är hudreaktion vid injektionsstället (ca 5%). I ARCH-studien (romosozumab vs. alendronat), sågs en överrisk av allvarliga kardiovaskulära händelser (2.0% vs. 1.1%). Däremot observerades ingen sådan överrisk i den större placebokontrollerade FRAME-studien (73). Den utökade övervakningen av Romosozumab togs bort av European Medicinal Agency 2025, då post authorization studies (PASS) inte visat på förhöjd kardiovaskulär risk. Romosozumab är dock fortsatt kontraindicerat vid tidigare hjärtinfarkt eller stroke.
Sällsynta biverkningar
Bisfosfonatbehandling medför ökad risk för osteonekros i käken (ONJ). Incidensen hos patienter med skelettmetastasering (som ges mycket högre doser) beräknas till 1-15%. Hos osteoporospatienter är incidensen nära den för allmänna befolkningen (0,001 till 0,01% jämfört med <0,001%) (74). Risken för ONJ vid behandling med denosumab liknar den vid bisfosfonater.
Risken för atypisk subtrokantär femurfraktur är förhöjd och ökar med behandlingsduration (3.2-50 fall per 100 000 personår). Risken för atypisk femurfraktur med denosumab liknar den för bisfosfonater.
Risk-nyttosambandet har bland annat beskrivits utifrån följande exempel: 5 års behandling med bisfosfonater hos 10 000 patienter resulterar i att 286 höftfrakturer och 859 kliniska frakturer undviks på bekostnad av 8 atypiska femurfrakturer (75, 76).
Läkemedelsbehandling hos äldre

Patienter som är äldre bör handläggas på samma sätt som yngre patienter. Utredningsgången anpassas efter patientens hälsostatus och förväntad överlevnad bör vägas in i utrednings- och behandlingsbeslut in hos de biologiskt allra äldsta. Då bentäthetsmätning kan vara svårt att få till stånd hos äldre och sköra patienter med kot- eller höftfrakturer, kan läkemedelsbehandling i lämpliga fall ges utan föregående mätning.
Tack vara långvarig effekt och god följsamhet är zoledronsyra speciellt lämpligt till denna grupp. Vid nedsatt njurfunktion rekommenderas denosumab, och då som tillsvidarebehandling.
Tillgänglig evidens talar för att äldre har lika stor nytta i form av minskad risk för fraktur av osteoporosläkemedel som yngre patienter. Lägre NNT (numbers needed to treat) med osteoporosläkemedel ses dock hos äldre pga. deras högre absoluta risk.
Innan insättande bör man utreda och vid behov inleda behandling för att korrigera eventuell hypokalcemi och vitamin D-brist.
Behandling efter en höftfraktur
I samband med höftfraktur bör behandling med osteoporosläkemedel ges om det inte finns kontraindikationer och behandlingen betraktas som adjuvantterapi. Behandlingsvalet styrs av patientens allmäntillstånd och där kan även ålder vara en faktor. Patienter under 50 år med höftfraktur bör bedömas av specialist då underliggande sjukdomar är vanliga. Hos de äldsta och ofta sköra är injektions- eller infusionsbehandling att föredra och ställningstagandet bör ske i direkt anslutning till vårdtillfället. Beslutet är beroende av hur vården är ordnad och vilka tidsramar och möjligheter som finns. Det är en fördel om första dosen kan administreras i samband med vårdtillfället. Vid korta vårdtider, kan därmed denosumab vara lämpligt läkemedel för de äldsta och sköraste patienterna. Det är möjligt att efter första injektionen av denosumab byta till zoledronsyra om det bedöms fördelaktigt, se nedan. Tidsaspekten är viktig hos dessa patienter eftersom risken för nya frakturer är mycket hög redan under de två första åren efter fraktur. Insättande av behandling bör därför ha skett inom fyra månader.
Denosumab har en mer gynnsam biverkningsprofil jämfört med zoledronsyra i nära anslutning till operation, eftersom man undkommer eventuella influensaliknande reaktioner relaterade till zoledronsyrainfusionen, vilka kan leda till förlängd vårdtid. Viktigt att man säkerställer uppföljning inom 6 månader för ställningstagande till fortsatt behandling med denosumab eller om det är lämpligt med byte till zoledronsyra. För yngre patienter med höftfraktur kan skelettanabol behandling vara motiverad. Dessa patienter bör utredas med DXA och remitteras till enhet som kan erbjuda sekventiell behandling.
Senast ändrad: 2 juni 2026