Vårdprogram
Vårdprogrammet är under uppdatering och beräknas vara helt färdigt i början på juni 2026
Läkemedelsbehandling bör alltid övervägas till:
- Patienter med nyligen genomgången eller tidigare fraktur i höft eller kota, oavsett bentäthet om det inte finns kontraindikationer
- Patient annan nyligen eller tidigare genomgången osteoporosrelaterad fraktur och hög frakturrisk (≥20% FRAX för osteoporosfraktur) samt låg bentäthet (≤-1 i T-score)
- Patienter med låg bentäthet (≤-2.5 i T-score) och hög frakturrisk (≥20% FRAX för osteoporosfraktur).
- Patienter med peroral kortisonbehandling (mer än motsvarande 5 mg prednisolon dagligen och förväntad behandlingstid överstigande 3 mån) särskilt vid ålder över 65 år, tidigare fragilitetsfraktur, bentäthet lägre än -1 i T-score, postmenopausala kvinnor
Inledning
Vårdprogrammet är utarbetat av Svenska Osteoporossällskapets styrelse 2020/2021
Kristian Axelsson
Ingrid Bergström
Sigridur Björnsdottir
Bo Freyschyss
Andreas Kindmark
Mattias Lorentzon
Eva Oskarsson
Katrin Rimsby
Märit Wallander
Kristina Åkesson
Datum för första versionen 2021-05-02
Skicka gärna synpunkter på vårdprogrammet. Epost: info@svos.se
Vårdprogrammet är utarbetat av Svenska Osteoporossällskapets styrelse 2020/2021
Kristian Axelsson
Ingrid Bergström
Sigridur Björnsdottir
Bo Freyschyss
Andreas Kindmark
Mattias Lorentzon
Eva Oskarsson
Katrin Rimsby
Märit Wallander
Kristina Åkesson
Datum för första versionen 2021-05-02
Skicka gärna synpunkter på vårdprogrammet. Epost: info@svos.se
Osteoporos är en folksjukdom som ökar risken för frakturer. I Sverige beräknas varannan kvinna och var femte man drabbas av en osteoporosrelaterad fraktur efter 50 års ålder. Många frakturer, framför allt kot- och höftfrakturer, medför ett betydande lidande, funktionsnedsättning, ökad dödlighet samt stora kostnader för sjukvården och samhället. De direkta och indirekta årliga kostnaderna för osteoporosfrakturer uppgår till 20 Mdr SEK. Ungefär 90 000 osteoporosrelaterad frakturer sker varje år och av dessa är ca 15 000 höftfrakturer.
Under 2020 har det utkommit tre nationella dokument; Nationella riktlinjer för rörelseorganens sjukdomar från Socialstyrelsen, Läkemedel vid osteoporos för att förhindra benskörhetsfrakturer från Läkemedelsverket och Personcentrerat och sammanhållet vårdförlopp Osteoporos – sekundärprevention efter fraktur från SKR, med slutversion till sjukvårdshuvudmännen för implementering 2021.
Socialstyrelsens nationella riktlinjer ger mycket hög prioritet att utreda och behandla frakturpatienter, vilket stärks av SKRs och därmed sjukvårdsregionernas prioritering att implementera ett sammanhållet vårdförlopp, vilket motsvarar frakturkedja. Det speglar att osteoporos fortfarande är både gravt underdiagnostiserat och underbehandlat i Sverige. Endast ca 14 % av kvinnor över 50 år får sekundärpreventiv läkemedelsbehandling inom 1 år efter sin osteoporosfraktur. Vid vissa sjukhus finns redan frakturkedjor för att förbättra de sekundärpreventiva insatserna, men samtidigt är behovet av vägledning och kompetensutveckling inom frakturprevention är stort i landet. Nyligen visades i en stor studie från fyra sjukhus i västra Sverige, att fler patienter blev utredda, fick läkemedelsbehandling medan färre drabbades av nya frakturer efter införande av frakturkedjor (1).
I samtliga rekommendationer framgår att alla patienter 50 år och äldre med osteoporosrelaterad fraktur ska riskvärderas, vid behov utredas och ges anpassade förebyggande åtgärder. Detta kommer troligen att leda till förbättrad utredning och behandling av osteoporos samt färre frakturer i framtiden.
Referenser
- Axelsson KF, Johansson H, Lundh D, Möller M, Lorentzon M. Association Between Recurrent Fracture Risk and Implementation of Fracture Liaison Services in Four Swedish Hospitals: A Cohort Study. J Bone Miner Res. 2020;35(7):1216-23.
Utredning
Vilka patienter kan vara aktuella för utredning och behandling av osteoporos?
Vilka patienter kan vara aktuella för utredning och behandling av osteoporos?
Osteoporospatienter finns inom de flesta specialiteter men framförallt inom allmänmedicin, ortopedi, geriatrik, endokrinologi och reumatologi.
Osteoporos kan identifieras inom tre olika huvudgrupper;
- patienter med en nyligen genomgången fraktur
- patienter som tidigare haft en fraktur som inte uppmärksammats eller blivit föremål för utredning
- patienter som inte haft någon fraktur men som har låg bentäthet och därmed hög risk att så småningom få en första fraktur.
Inom alla grupper kan finnas patienten som har en underliggande orsak till osteoporos, dvs sekundär osteoporos. Det betyder att patienterna kommer in i sjukvården via olika vägar; genom ortopedisk akutklinik, primärvården där man upptäcker riskfaktorer eller via annan specialitet på grund av sin grundsjukdom.
Sekundärprevention genom systematisk och strukturerad identifiering inom ramen för en frakturkedja och med hjälp av en frakturkoordinator (osteoporoskoordinator) syftar i första hand på att snabbt hitta och initiera förebyggande åtgärder hos de som nyligen genomgått en fraktur, inte minst för att dessa har en mycket hög risk för nya frakturer inom bara något år.
Primärprevention syftar till att identifiera och behandla de som ännu inte haft någon fraktur, det kan vara svårare och bygger på att man känner till och frågar om riskfaktorer men är särskilt viktigt när det gäller de med andra sjukdomar som är kopplade till hög risk.
Den stora gruppen av patienter som är viktigast att utreda för misstänkt osteoporos är de som redan har råkat ut för en första osteoporosrelaterad fraktur, nyligen eller tidigare, för att minska risken för nya frakturer. En annan stor patientgrupp är de som är aktuella för behandling med kortison peroralt.
Med osteoporosrelaterade frakturer menas frakturer som oftast uppstått vid låg belastning såsom fall i samma plan eller vid annan låg energi, men det är bättre att vara inkluderande eftersom energinivån kan vara svår att skatta. Andra benämningar kan också vara osteoporosfraktur, lågenergifraktur, fragilitetsfraktur eller benskörhetsfraktur. Typiska osteoporosrelaterade frakturer är fraktur i handled, överarm, bäcken, höftled och kota.
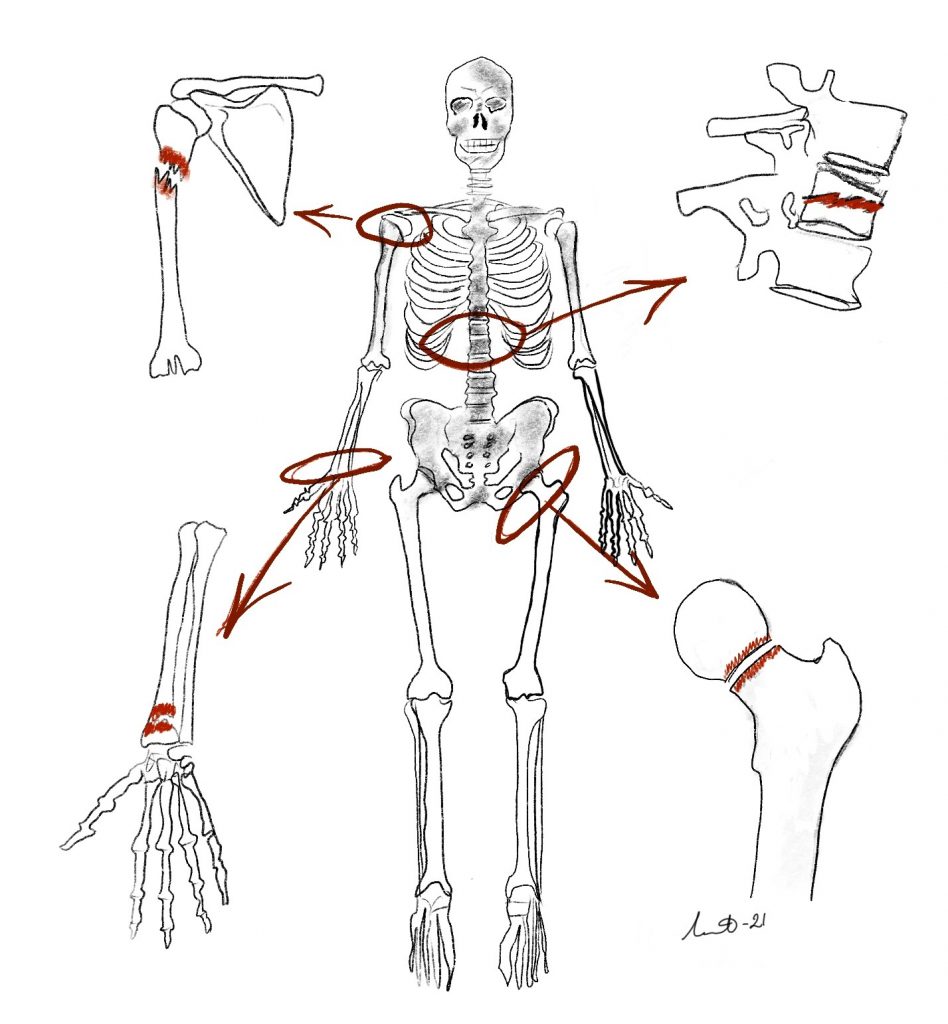
Syftet med osteoporosutredning är att:
- Identifiera patienter med hög frakturrisk
- Uppskatta risken för framtida fraktur
- Utreda eventuell förekomst av sekundär osteoporos
- Göra en sammanfattande bedömning och förslag om lämplig behandling
- Formulera en uppföljningsplan
Riskvärdering
Riskvärderingen måste vara individuell och ta hänsyn till patientens hela riskprofil. Det innebär att särskilt ålder och genomgången fraktur spelar stor roll. I många fall har patienten uppenbart hög frakturrisk och behandling är tydligt motiverad. Detta gäller tex äldre patienter med kotkompression, höftfraktur eller som ska få kortisonbehandling i hög dos och äldre patienter med fraktur i kombination med andra riskfaktorer.
I andra fall är indikationen för utredning och behandling inte lika tydlig. Kvantifiering av risk kan göra med olika verktyg, där FRAX är det mest använda. Vid en initial riskvärdering behöver FRAX kompletteras för att täcka särskilt fallbenägenhet och annan sjuklighet.
Fracture Risk Assessment Tool, (FRAX) en webbaserad riskkalkylator för beräkning av absolut risk för höftfraktur och osteoporosfraktur (kot-, underarms-, höft- eller skulderfraktur. FRAX kan användas utan eller med bentäthetsvärde från lårbenshals (1).
FRAX kan användas hos män och kvinnor 40-90 år gamla, men uppskattningen av frakturrisken är beräknad på behandlingsnaiva individer och avspeglar sannolikt inte en korrekt risk om personen har eller har haft behandling med osteoporosläkemedel. FRAX-risken är starkt beroende av ålder vilket exemplifieras i tabellen. Exemplen i tabell 1 visar också att fraktur och kortison tillhör de starkast riskfaktorerna medan rökning spelar mindre roll.
FRAX har begränsningar och tar bland annat inte hänsyn till frakturtyp (t.ex. tidigare kotfraktur medför ökad risk jämfört med andra frakturer), antal tidigare frakturer (fler frakturer ökar risken mer än en fraktur), tid sedan fraktur (frakturrisken är högst nära inpå frakturen och avtar med tiden), bentäthetsvärde i ländrygg, fallrisk , dosen av kortison, antal cigaretter eller mängden alkohol per dag. Vid en skattning av risk bör man därför väga in om patientens samlade riskbild ökar eller minskar den uppskattade risken med FRAX (2). I ett gränsfall för behandling baserat på FRAX, bör förekomst av någon eller flera av riskfaktorerna ovan väga över för beslut om behandling.
| Exempel | Osteoporosfraktur | Höftfraktur |
| 58-årig kvinna inga riskfaktorer | 6.9% | 1.4 % |
| 58-årig kvinna med radiusfraktur | 15% | 4.3% |
| 58-årig kvinna med radiusfraktur och hereditet för höftfraktur | 25% | 5.6% |
| 58-årig kvinna med radiusfraktur och rökare | 17% | 6.4% |
| 58-årig kvinna med radiusfraktur, rökning, kortison | 28% | 13% |
| 67-årig kvinna inga riskfaktorer | 13% | 4.2% |
| 67-årig kvinna med radiusfraktur | 24% | 9.5% |
| 67-årig kvinna med radiusfraktur och hereditet för höftfraktur | 38% | 15% |
| 67-årig kvinna med radiusfraktur och rökare | 28% | 14% |
| 67-årig kvinna med radiusfraktur, rökning, kortison | 44% | 26% |
| 78-årig kvinna inga riskfaktorer | 25% | 15% |
| 78-årig kvinna med radiusfraktur | 39% | 23% |
| 78-årig kvinna med radiusfraktur och hereditet för höftfraktur | 65% | 57% |
| 83-årig kvinna inga riskfaktorer | 30% | 18% |
| 83-årig kvinna tidigare radiusfraktur | 43% | 26% |
| 88-årig kvinna inga riskfaktorer | 28% | 16% |
| 88-årig kvinna tidigare radiusfraktur | 40% | 24% |
| 88-årig kvinna tidigare radiusfraktur, hereditet, kortison | 72% | 68% |
| *Längd 167, vikt 60 |
Klinisk basutredning vid osteoporos
Anamnes
Anamnes och status tas på sedvanligt sätt inkluderande tidigare/nuvarande sjukdomar mm, men några punkter är av särskild vikt för bedömning av osteoporospatienter:
- Riskfaktoranamnes är central vid ställningstagande till utredning/behandling. Hur väl förklarar totalbilden patientens benmassa, behövs ytterligare utredning, hur stor är frakturrisken? På många enheter används en självifylld enkät för de viktigaste riskfaktorerna, vilket underlättar faktainsamling. (Riskfaktorer för fraktur – se faktaruta 1)
- Vid oväntat låg benmassa kompletteras anamnes med frågor kring potentiella orsaker till sekundär osteoporos
- Detaljer om när, hur och var frakturer uppstått är viktigt för att bedöma risk och om de är av lågenergikaraktär.
- Det är viktigt framförallt hos äldre patienter och patienter med multipla kotkompressioner att få en uppfattning om pats förmågor och aktivitetsnivå med betoning på självständighet/hemtjänst/hemsituation, gångförmåga/gånghjälpmedel/fallrisk. Egen träning inklusive balansträning bör efterfrågas.
- Ryggvärk och längdminskning bör efterfrågas
- Läkemedel, och framförallt läkemedel som påverkar skelettet negativt se nedan.
- Levnadsvanor, nutrition vid lågt BMI, intag av mejeriprodukter (kalciumintag). Rök- och alkoholvanor.
- Inför behandling med antiresorptiva bör eventuella dentala problem och framförallt planerade ingrepp (tandextraktioner/implantat) efterhöras.
| Hög ålder | Låg bentäthet |
| Tidigare fraktur (antal, typ och när de inträffade) | Falltendens, fallrädsla, dålig balans |
| Hereditet: diagnosticerad osteoporos, kot- eller höftfraktur hos förälder. Syskon med osteoporos. | Fysisk inaktivitet |
| Läkemedel som påverkar skelettet: p.o. kortison, antihormonell behandling (vid bröst- eller prostatacancer), antiepileptika, protonpumpshämmare. | Läkemedel som ökar fallrisken: hypnotika (sömnläkemedel, lugnande läkemedel), opioider, hypertoniläkemedel, SSRI. |
| Sjukdomar kopplade till sekundär osteoporos (t.ex. reumatoid artrit, diabetes mellitus typ I, osteogenesis imperfecta, hypertyreos m.fl.) | BMI < 19 kg/m2 eller viktnedgång > 10 kg sedan 25 års ålder, uttalad viktnedgång efter obesitas kirurgi |
| Tidig menopaus (<45 års ålder) | Rökning (mängd cigaretter och tid som rökare) |
| Sjukdomar som leder till ökad fallrisk: Parkinson, demens, stroke | Alkoholöverkonsumtion (>3 standardglas om dagen) |
Status
- Aktuell längd och längdminskning (>3 cm om under 70 år, > 5 cm om 70 år)
- Rygg – kyfosutveckling (undersök avstånd mellan höftbenskam revbensbåge)
- Fokus på allmäntillstånd, vikt, balans, gångförmåga, tecken på tidigare operationer, nutritionsstatus, sekundär osteoporos.
Laboratorieprover
I de flesta fall har patienten låg benmassa pga. ärftlig benägenhet och/eller faktorer som är kända redan inför läkarbesöket eller känd annan sjukdom. Laboratorieutredning utförs för att inte missa en okänd bakomliggande sjukdom, samt för att utvärdera njurfunktion och serum kalcium och D-vitaminstatus inför val av behandling.
Basal standard-utredning: Hb, SR, P-calcium, albumin, S-25-OH vitamin D, PTH, ALP (ofta förhöjt under frakturläkning), kreatinin/eGFR, hos män även S-testosteron (om förekomst av symtom som tyder på testosteronbrist eller uttalad sänkning av benmassa av oklar anledning).
Vid oväntat låg benmassa eller oförklarliga frakturer utvidgas utredningen med ledning av anamnes, status och basala labprover för att utesluta eller diagnosticera sekundär osteoporos, se nedan.
Ställningstagande till bentäthetsmätning
Bentäthetsmätningen ska bara göras om det påverkar den fortsatta handläggningen såsom val av behandling eller behandlingslängd. Bentätsmätningen ger ett utgångsvärde, vilket är särskilt värdefullt och nödvändigt om man förväntar sig att uppföljande mätningar kan bli aktuella.
För vilka patienter ska utredning med bentäthetsmätning övervägas:
- Kot- eller höftfraktur, om mätningen påverkar fortsatta handläggningen (behov av utredning respektive val av läkemedelsbehandling)
- Planerad eller pågående systemisk högdos kortisonbehandling, (helst före eller tidigt under behandlingen) som väntas pågå i mer än tre månader
- Riskfaktorprofilen indikerar hög risk pga. frakturer eller andra riskfaktorer. För att uppskatta frakturrisken kan FRAX användas som vägledning. Socialstyrelsen har tidigare rekommenderat en risk om minst 15% för osteoporosfraktur inom 10 år som lämplig gräns för att utföra en DXA-mätning.
- Vid sjukdom eller läkemedelsbehandling där man har anledning att misstänka utveckling av osteoporos. Vid ett flertal sjukdomar eller vid viss typ av medicinering är osteoporos en vanlig komplikation på grund av specifik skelettpåverkan och/eller låg belastning, malnutrition och allmän sjukdom.
- Hos vissa patienter kan det Ibland vara motiverat att påbörja behandling; 1) utan att planera för DXA mätning exempelvis äldre patient med höftfraktur där behandlingsindikation är uppenbar; 2) innan svar har kommit från DXA mätningen exempelvis vid mycket hög dos systemisk kortisonbehandling till postmenopausala kvinnor och äldre män eller 3) för biologiskt äldre, där det kan vara svårt att genomföra DXA-mätning och där resultatet inte bedöms påverka behandlingsindikationen.
Bentäthetsmätning med central DXA ländrygg och höft
Mätning med central DXA utförs i ländrygg och i höft. Resultatet ger ett utgångsvärde för ställningstagande till behandling, val av behandling samt för uppföljning av behandlingseffekt. Oväntat låg benmassa indikerar även behov av en eventuell utredning avseende sekundär osteoporos, se nedan.
Eftersom DXA-mätningen tillsammans med övriga riskfaktorer skall ligga till grund för en uppskattning av patientens frakturrisk bör information om riskfaktorer för fraktur ingå i remiss till DXA-mätning. Ange i remissen kända frakturer eller operationer i mätområdena.

För postmenopausala kvinnor och män över 50 år ges svar i T-score (uttryckt i standarddeviationers skillnad mellan patientens värde och unga friska kvinnors medelvärde). T-score utgör alltså här underlag för diagnos och för behandlingsindikation. För övriga patienter ges svaret i Z-score (uttryckt i standarddeviationers skillnad mellan patientens värde och ålders- och könsmatchades medelvärde).
| T-score | Tolkning | |
|---|---|---|
| T-score > – 1.0 | Normal bentäthet | |
| T-score -1.0 – 2.5 | Osteopeni | |
| -1.0 – -1.5 | Lätt sänkt bentäthet men nära normal | Sällan indikation för behandling men beroende på andra riskfaktorer. |
| -1.5 – -2.0 | Måttlig sänkt bentäthet | Behandlingsindikation beroende på andra risk faktorer och ofta vid fraktur eller kortisonbehandling |
| -2.0 – -2.5 | Uttalat sänkt bentäthet och nära osteoporos | Ofta behandlingsindikation särskilt i samband med fraktur |
| T-score ≤-2.5 | Osteoporos |
I regel görs uppföljande mätningar tidigast efter två år och inte tätare än vart annat år, p.g.a. vanligtvis små förväntade förändringar och mätningens felmarginal. Kortare intervall kan användas vid t.ex. insättning av p.o. kortison och vid avslutande av teriparatid eller romosozumab (18-24 respektive 12 månader).
Förändringar i bentäthet kontrolleras i ländrygg (kota L1-L4) och i total höft, mäts över tid och anges ges i procent förändring av bentäthet i g/cm2 (man skall ej ange förändring i T-score). Vid upprepad mätning ska svaret alltid innehålla information om det skett en signifikant förändring av bentätheten sedan föregående mätning eller inte. För att en förändring ska betraktas som signifikant bör den överstiga 2-3 %.
OBS! Vid uppföljande mätningar ska patienten första hand remitteras till samma mottagning då man inte med säkerhet kan jämföra mätningar gjorda på olika maskiner/mottagningar.
Om man bedömer att uppföljande mätning inte kommer påverka insatt behandling och om följsamheten är god kan uppföljningstiden förlängas. Likaså kan man avstå från uppföljande mätning hos äldre patienter med god följsamhet om det inte påverkar fortsatt behandlingsindikationer eller behandlingavslut.
Personal som utför och tolkar DXA-mätningar bör ha erforderlig utbildning och certifiering från International Society for Clinical Densitometry (ISCD/IOF), för att säkerställa god reproducerbarhet och tillräcklig mätkvalitet på undersökningarna. Här kan du läsa om kurser som SVOS erbjuder för att uppnå kompetens och certifiering i DXA-mätningar/tolkningar.
Vertebral fracture assessment (VFA)
Måttliga och uttalade kotkompressioner inom området Th6-L4 kan i de flesta fall identifieras med god precision med hjälp av DXA-maskinen med patienten i sidoläge, s.k. VFA. Eftersom förekomst av kotfrakturfraktur kraftigt ökar risken för framtida fraktur bör VFA ingå som rutin för de flesta patienter vid DXA-mätning. VFA minskar behovet av konventionell röntgen då kotfrakturer kan identifieras och i många fall behöver utredningen inte kompletteras med ytterligare radiologi.
Röntgen bröst- och ländrygg
Patient med misstänkt kotkompression (ryggsmärtor och/eller längdminskning) ska i första hand utredas med röntgen bröst- ländrygg, eller lågdos CT vid enheter där detta rekommenderas. Vid skolios, utförs datortomografi. VFA i samband med DXA-undersökning kan, i många fall, numera ge tillräcklig information. Vid misstanke på neurologisk påverkan eller om mer omfattande kartläggning är motiverad, används MR. MR kan också användas vid oklarhet huruvida en kotfraktur är gammal eller nytillkommen.
Referenser
- Kanis JA, Hans D, Cooper C, et al. Interpretation and use of FRAX in clinical practice. Osteoporos Int. 2011;22:2395-411.
Sekundär osteoporos
Tidigare okänd sekundär osteoporos ska misstänkas och utredas särskilt hos män under 65 år och kvinnor före eller tidigt i menopaus med fraktur och låg bentäthet utan kända riskfaktorer eller sjukdomar.
Yngre patienter med höftfraktur efter lågenergitrauma (<60 år) bör remitteras för utredning vid osteoporosenhet då sekundära orsaker är vanligt förekommande.
Z-score (som är korrigerat för ålder och kön) utanför referensområdet (< -2, dvs 2 standarsavvikelser) utan uppenbar förklaring indicerar också ofta utökad utredning avseende sekundär osteoporos.
Vid anemi, hög SR eller annan misstanke på myelom kontrolleras P-elektrofores och U-elektrofores alternativt fria lätta kedjor S-FLC. Transglutaminas-antikroppar och IgA i serum kontrolleras vid celiakimisstanke, tex GI-besvär eller tecken på tex järnbrist.
Utredning för andra ännu mer ovanliga tillstånd kan ibland utföras vid oförklarligt mycket låg bentäthet eller oförklarlig uttalad frakturbenägenhet.
Sekundär osteoporos kan mycket väl handläggas i primärvården, inte minst i samband med kortisonbehandling, men vid tveksamheter så rekommenderas kontakt med endokrinmottagning/osteoporosspecialist.
| Läkemedel: framförallt p.o. glukokortikoider och aromatashämmare; även cytostatika, cyklosporin, litium, GnRH-agonister, antiepileptika, heparin | Kroniska inflammatoriska sjukdomar: t ex reumatoid artrit, KOL, inflammatorisk tarmsjukdom |
| Östrogenbrist hos yngre kvinnor (primär eller sekundär amenorré – vanliga orsaker är läkemedel, hård träning eller anorexia nervosa) | Malnutrition och malabsorption, celiaki, mag-tarmoperation (gastric bypass), extremkost |
| Endokrina rubbningar: t ex hyperparatyroidism, hypertyreos, hypogonadism, Cushings syndrom, hypofosfatemi | Hematologiska sjukdomar: tex Multipelt myelom, mastocytos |
| Alkoholism | Lever- och njursvikt |
| Genomgången transplantation | Andra tillstånd som medfört malnutrition och immobilisering |
| Medfödda bindvävssjukdomar OI, EDS |
Kortison och osteoporos
Kortisonbehandling i hög-dos är den vanligaste orsaken till sekundär osteoporos. Under första året av behandlingen minskar bentätheten med cirka 12% med följt av något mer långsam årlig minskning med omkring 3%. Mellan 30-50% av patienterna med långtidskortisonbehandling får frakturer, och de uppkommer oftast under första behandlingsåret.
Kotkompressioner är en av de mest fruktade biverkningarna av kortisonbehandling och det är svårt att förutsäga vem som kommer att drabbas. Frakturrisken är dosberoende och ökar inom 3-6 månader efter insatt kortisonbehandling, men det finns en individuell variation i känslighet för kortison, där yngre personer inte förlorar benmassan lika snabbt som äldre.
Bisfosfonat bör ges till riskpatient vid behandling motsvarande prednisolon ≥ 5 mg/dag med förväntad behandlingstid >3 månader. Den största benförlusten sker tidigt och snabbt. Därför är det viktigt att sätta in förebyggande behandling i princip samtidigt som kortisonet, även om man inte är säker på hur lång behandlingstiden kommer bli och oavsett om eventuellt DXA svar föreligger.
Fertila kvinnor och män under 50 år bör inte få Bisfosfonat utan mycket starka skäl, såsom tidigare kotkompression, och bör remitteras till specialist på benmetabol sjukdom (1). Vid användning av inhalationssteroider i samband med astma kan också finnas en riskökning för osteoporos och fraktur vid långtidsbehandling med höga doser (2).
Osteoporos vid kronisk njursvikt
Njurfunktionen försämras med stigande ålder och en hög andel av äldre har kronisk njurinsufficiens av en grad som måste beaktas vid riskbedömning och behandlingsbeslut (3). Patienter med senare stadier av kronisk njurinsufficiens (CKD), framför allt grad 4-5 har en förhöjd risk för framför allt perifera frakturer beroende på ett flertal faktorer (4).
Dessa inkluderar negativa effekter på skelettet av sjukdomen i sig dvs uremiska toxiner, acidos, minskad fysisk aktivitet och nutritionsproblematik. Patienterna kan ha ett flertal läkemedel med negativ effekt på skelettet som kortison, protonpumpshämmare och loopdiuretika. Dessutom förekommer oftast komplexa skelettmetabola störningar sekundärt till avancerad njursjukdom så kallad Chronic Kidney Disease Mineral Bone Disease (CKD-MBD), tex sekundär hyperparathyroidism, osteomalaci och adynamisk bensjukdom.
Uppskattning av frakturrisk vid kronisk njurinsufficiens
Trots den komplexa bilden kan man använda sedvanliga riskfaktorer för att uppskatta frakturrisken även vid svår CKD. De vanliga riskfaktorerna kvinnligt kön, ålder, tidigare fraktur, kortisonbehandling m.fl. utgör riskfaktorer även i denna population. DXA (i första hand höft och ländrygg) och FRAX kan användas för att uppskatta frakturrisken. Man bör beakta att CKD stadium 4-5 ytterligare ökar risken för fraktur utöver vad riskfaktorerna indikerar och att frakturrisken sannolikt är högre än den uppskattade (4).
Behandling av osteoporos vid uttalad kronisk njurinsufficiens
Det vetenskapliga underlaget för behandling av osteoporos hos patienter med GFR < 30 ml/min är undermåligt och inga prövningar med fraktur som endpoint har specifikt studerat denna grupp. Patienter med uttalad njurinsufficiens och hög frakturrisk/osteoporos rekommenderas liksom andra patienter med osteoporos fysisk aktivitet, adekvat nutrition och ett totalt kalciumintag av cirka 1000-1200 mg per dag via mat och/eller läkemedel.
Som regel behandlas osteoporos ned till GFR cirka 25 ml/min i frånvaro av CKD-MBD ungefär på samma sätt som osteoporos hos njurfriska dock med beaktande av att de flesta läkemedel är kontraindicerade vid GFR < 30 ml/min.
Den skelettmetabola situation vid kronisk njurinsufficiens i senare stadier CKD 4-5 (GFR < 30 ml/min), är komplex och innefattar ett flertal olika tillstånd/mekanismer som behöver beaktas inför ställningstagande till behandling. Detta ligger inte inom ramen för SVOS rekommendationer. I första hand skall patientens uremi respektive CKD-MBD behandlas av specialist i njurmedicin.
Randomiserade studier med fraktur som effektmått på denna patientgrupp (GFR<30) saknas. Ett relativt litet antal patienter med GFR mellan 30 och 15 ml/min inkluderades framför allt i två randomiserade frakturstudier (en med risedronat och en med denosumab denosumab) och effekten av läkemedlen på dessa patienter har analyserats i efterhand, sk post hoc (5-6). I dessa kohorter var S-Calcium och S-PTH normala, vilket oftast inte är fallet vid GFR <30. Sammanfattningsvis baserat på dessa få patienter, föreföll behandlingseffekten av denosumab (n=70) respektive risedronat (n=572) likartad med effekten på övriga patienter i studierna, med en signifikant minskning av antalet kotkompressioner. Patientantalet var för litet för att bedöma effekten på icke vertebrala frakturer. Baserat på dessa data rekommenderas behandling av osteoporos ned till GFR cirka 25 ml/min i de flesta riktlinjer.
Vid GFR lägre än 30 ml/min är denosumab det enda osteoporosläkemedel som inte är kontraindicerat enligt FASS-texterna. Zoledronsyra och alendronat är kontraindicerade under 35 ml/min och risedronat liksom raloxifen och teriparatide under 30 ml/min.
Referenser
- Weinstein RS. Clinical practice. Glucocorticoid-induced bone disease. N Engl J Med. 2011;365(1):62-70.
- Chalitsios CV, Shaw DE, McKeever TM. Risk of osteoporosis and fragility fractures in asthma due to oral and inhaled corticosteroids: two population-based nested case-control studies. Thorax. 2021;76(1):21-8.
- Malmgren L, McGuigan FE, Christensson A, Akesson KE. Longitudinal Changes in Kidney Function Estimated from Cystatin C and Its Association with Mortality in Elderly Women. Nephron. 2020;144(6):290-8.
- Evenepoel P, Cunningham J, Ferrari S, Haarhaus M, Javaid MK, Lafage-Proust MH, et al. European Consensus Statement on the diagnosis and management of osteoporosis in chronic kidney disease stages G4-G5D. Nephrol Dial Transplant. 2021;36(1):42-59.
- Jamal SA, Ljunggren O, Stehman-Breen C, Cummings SR, McClung MR, Goemaere S, et al. Effects of denosumab on fracture and bone mineral density by level of kidney function. J Bone Miner Res. 2011;26(8):1829-35.
- Miller PD, Roux C, Boonen S, Barton IP, Dunlap LE, Burgio DE. Safety and efficacy of risedronate in patients with age-related reduced renal function as estimated by the Cockcroft and Gault method: a pooled analysis of nine clinical trials. J Bone Miner Res. 2005;20(12):2105-15.
Farmakologisk behandling
Vårdprogrammet är under uppdatering och beräknas vara helt färdigt i början på juni 2026
Frakturförebyggande åtgärder och behandling
Att förebygga frakturer utgår från de två viktigaste riskfaktorerna – att stärka skelettet och att förhindra fall.
Idag finns effektiva läkemedel för att stärka skelettet medan fysisk träning och belastning av skelettet bidrar till att i första hand bibehålla skelettets egenskaper. Fallprevention är ett vidare begrepp som innefattar flera modaliteter; både att stärka den fysiska förmågan, balans och koordination som att undanröja risker som kan bidra till fall. Dessa risker är både relaterade till person och till den externa miljön och behöver anpassas varje patients förutsättningar
Vilka ska ha läkemedelsbehandling? Beslut om benspecifik behandling ska grundas på en samlad klinisk värdering, baserat både på bentäthetsvärden, uppskattning av frakturrisken, patientens hälsotillstånd, eventuella sekundära orsaker och värdering av nytta vs. risk för biverkningar. Ju högre frakturrisk desto starkare behandlingsindikation.
Ingången för ställningstagande till behandling baseras ofta på hur patienten identifieras: 1) nyligen genomgången fraktur där patienten identifieras via frakturkedjan, 2) tidigare genomgången fraktur där patienten inte identifieras inom en frakturkedja och frakturen kan ligga relativt nära i tid eller för många år sedan eller som vid kotfraktur, uppmärksamma längdminskning eller kronisk ryggsmärta eller 3) inga frakturer och identifieras genom riskfaktorer eller vid andra sjukdomar.
Åldersberoende interventionsgränser
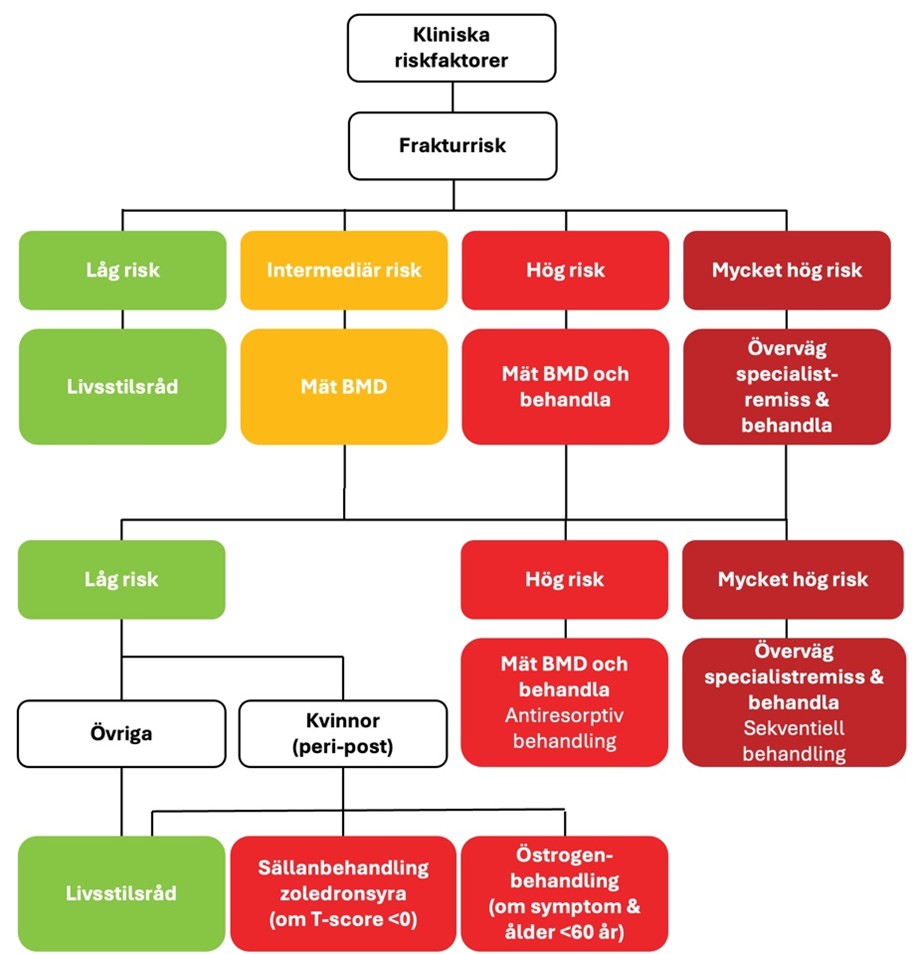
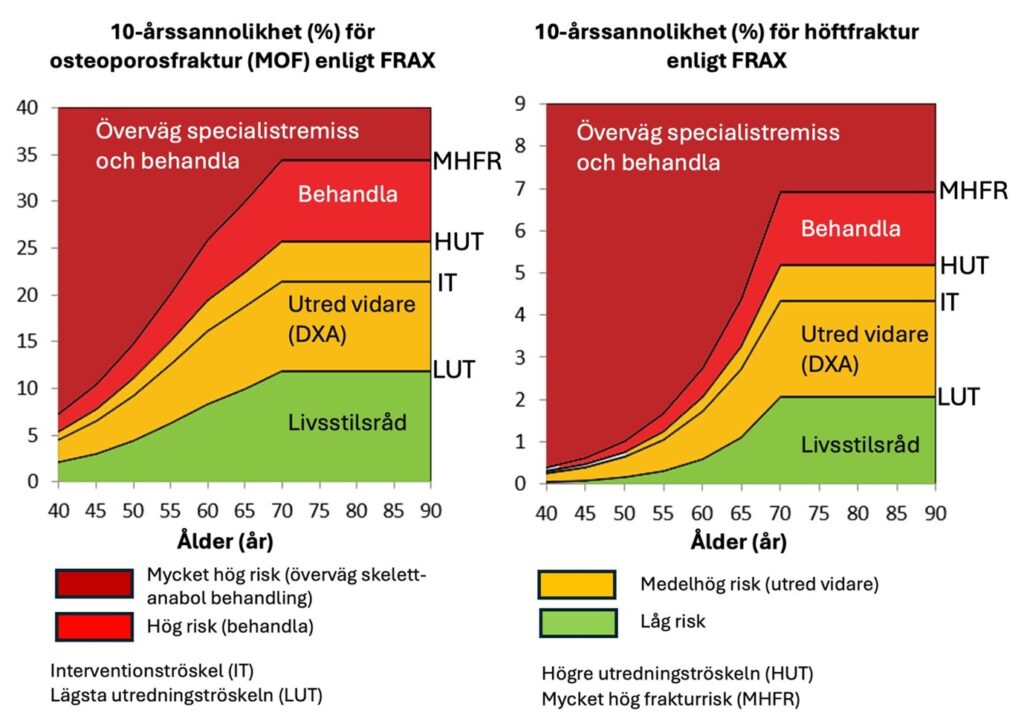
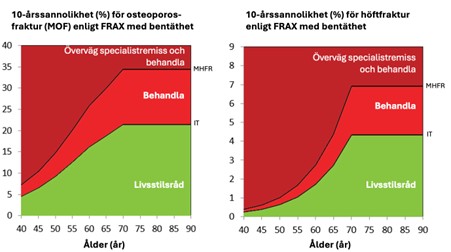
Den sannolikhet som krävs för att behandling ska vara motiverad, den s.k. interventionsgränsen, definieras som sannolikheten för ny fraktur hos en postmenopausal kvinna med tidigare fraktur vid en given ålder. Även om frakturrisken inom 10-år (enligt FRAX) hos en kvinna med osteoporos i 55-årsåldern är mycket lägre än för en kvinna med samma tillstånd i 70-års ålder, är livstidrisken för fraktur hos den yngre kvinnan mycket hög. Risken för höftfraktur för kvinnor med osteoporos och yngre än 70 år överstiger 27% under en 25-årsperiod (45). Utan intervention förväntas bentätheten successivt minska med ökande ålder vilket bidrar till den gradvisa ökningen av frakturrisken. Det är därför högst rimligt att hos patienter med låg bentäthet förbättra bentätheten och därmed minska frakturrisken på lång sikt. Val av behandling avgörs av ålder, bentäthet och frakturrisk. Eftersom frakturrisken påverkas av åldern, sätts den åldersberoende interventionsgränsen lägre hos yngre än hos äldre kvinnor för att långsiktigt minska deras frakturrisk (Figur 1 och Tabell 1). Val av behandling och behandlingsintervall beror på hur nedsatt bentäthen är och hur hög frakturrisken är (se avsnitt om Farmakologisk behandling).

Figur 1.
Osteoporosfraktur (MOF) – gränser för 10-årssannolikheter (%)
Tabell
Höftfraktur – gränser för 10-årssannolikheter (%)
Tabell
Figur 1 och tabell 1. Åldersberoende 10-årssannolikheter (%) och gränser för utredning och behandling för osteoporosfraktur (vänster) och höftfraktur (höger) enligt FRAX för Sverige. IT=Interventionströskeln, LUT=Lägsta utredningströskeln, HUT=Högre utredningströskeln. MHFR=Mycket hög frakturrisk. Illustrationer som anpassats från (1).
Hos yngre postmenopausala kvinnor, som slutat menstruera nyligen (de senaste 10 åren), kan man under vissa villkor överväga hormonersättningsbehandling, alternativt infusion zoledronsyra med varierande förlängt behandlingsintervall (se efterföljande stycke).
En första riskbedömning kan göras utifrån kliniska riskfaktorer, ålder och kön, enligt Figur 1. För personer med risk som överstiger den lägsta interventionströskeln för utredning med DXA bör remitteras för bentäthetsmätning, för att 1) ge vägledning till om behandling ska ges och 2) för att avgöra typ av behandling, då skelettanabol behandling bör övervägas vid mycket hög frakturrisk (44) eller mycket låg bentäthet. Med hjälp av bentäthetsvärdet kan en ny FRAX-bedömning utföras där bentäthet i lårbenshalsen tas med vilket ger en säkrare frakturriskbedömning (Figur 2).
Behandlingsindikation
Behandling med osteoporosläkemedel bör alltid övervägas till:
- Patienter med nyligen genomgången eller tidigare fraktur i höft eller kota, oavsett bentäthet om det inte finns kontraindikationer
- Patient annan nyligen eller tidigare genomgången osteoporosrelaterad fraktur och hög frakturrisk (≥20% FRAX för osteoporosfraktur) samt låg bentäthet (≤-1 i T-score)
- Patienter med låg bentäthet (≤-2.5 i T-score) och hög frakturrisk (≥20% FRAX för osteoporosfraktur).
- Patienter med peroral kortisonbehandling (mer än motsvarande 5 mg prednisolon dagligen och förväntad behandlingstid överstigande 3 mån) särskilt vid ålder över 65 år, tidigare fragilitetsfraktur, bentäthet lägre än -1 i T-score, postmenopausala kvinnor
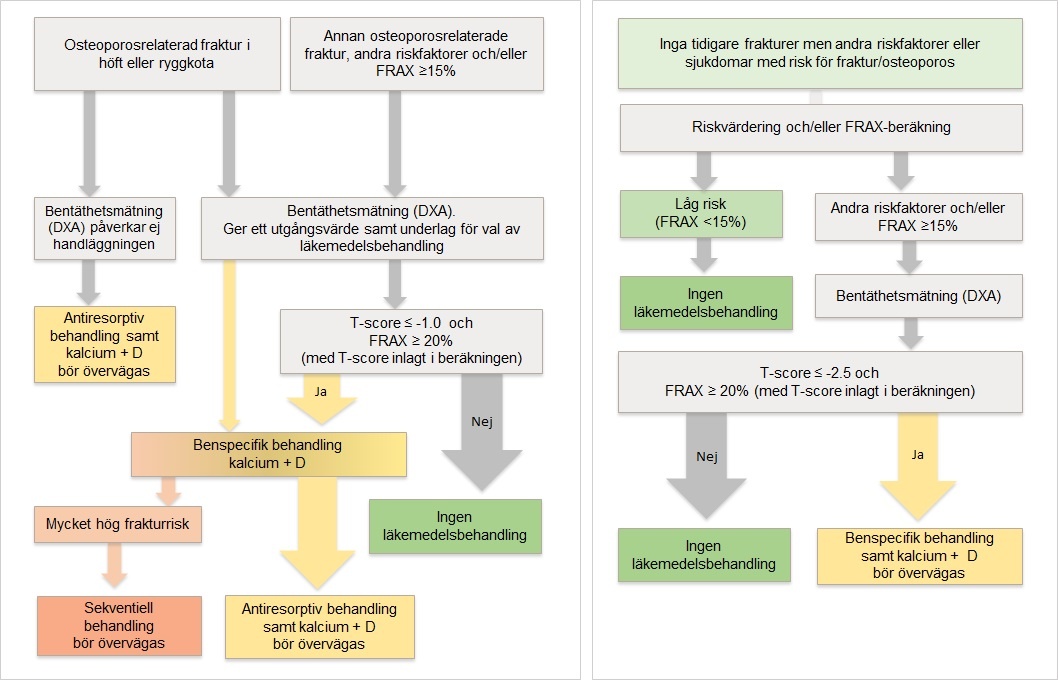
Läkemedelsbehandling
Basbehandling med kalcium och vitamin D
Benspecifika läkemedel ska i de allra flesta fall kombineras med tillskott av kalcium och vitamin D. Kalcium och vitamin D (kolekalciferol) ges som tillägg till annan benspecifik läkemedelsbehandling om tillräckligt intag (adekvat dagligt intag av kalcium: 800 mg och för D-vitamin: 800 IE) inte kan säkerställas. Eftersom den frakturförebyggande effekten är otillräcklig/tveksam används kalcium och vitamin D ej enskilt eller i kombination, som monoterapi vid osteoporos.
Tips: Påbörja behandling med kalcium-Vitamin D 500 mg + 400-800E /dag 1-2 veckor innan benspecifik behandling. Det underlättar i att bedöma om eventuella gastrointestinala biverkningar är relaterade till kalcium snarare än det specifika läkemedlet.
Efter avslutad behandling med bisfosfonater kan man fortsätta med kalcium och vitamin D om konstaterad brist på kalcium och D-vitamin eller om tillräckligt intag inte kan säkerställas vid kostanamnes.
Benspecifika läkemedel
Benspecifika läkemedel definieras som antingen antiresorptiva (hämmar osteoklasternas aktivitet) eller anabola (stimulerar osteoblaster till ny benbildning). Läkemedlens effekt i form av riskreduktion för frakturer är väl dokumenterad. Samtliga läkemedel nedan är godkända för behandling av både kvinnor och män med ökad risk för fraktur (med undantag för romosozumab). Val av läkemedel avgörs av bedömning av patientens risk och totala hälsosituation samt eventuella biverkningar. Följsamheten är betydligt bättre vid parenteral än vid per oral osteoporosbehandling.
Antiresorptiva läkemedel – bisfosfonater och denosumab
Bisfosfonater
Bisfosfonater är förstahandsbehandling i de flesta fall enligt nationella och internationella rekommendationer. I stora, randomiserade placebokontrollerade studier minskar både alendronat och zoledronsyra (de vanligen använda bisfosfonaterna) risken för kot-, höftfraktur och andra frakturer jämfört med placebo, hos postmenoapausala kvinnor med låg bentäthet. Riskminskningen har varit cirka 50%-70% för kotfrakturer, cirka 40% för höftfrakturer och cirka 20% för övriga frakturer i 3-åriga studier på högriskpatienter (1-3).
Behandling med alendronat och zoledronsyra förutsätter att kreatininclearence är 35 ml/min eller högre varför kreatinin måste kontrolleras inom 3 månader före behandling. Även s-kalcium, 25-OH-D-vitamin och PTH bör kontrolleras, eftersom antiresorptiv behandling är olämplig vid obehandlad hypokalcemi och D-vitaminbrist skall korrigeras före behandling.
Alendronat, 70 mg tablett 1 ggr/ vecka
Initialt behandlas patienten under 3-5 år, vanligen 5 år. Därefter tar man ställning till fortsatt behandling baserat på patientens riskprofil och bentäthet.
Om patienten haft mer än en kotkompression eller har kvarstående osteoporos i höft (T-score < -2,5) fortsätter man vanligen behandlingen i upp till maximalt 10 år.
Efter utsatt alendronat kan man göra ny DXA efter 3 år och därefter 2 år om återinsättning kan bli aktuell. Vid signifikant sjunkande bentäthet återinsätts alendronat under cirka 3 år. Alendronat bör återinsättas efter 5 år oavsett om bentätheten sjunkit och då under 3 års tid och därefter upprepas proceduren.
Alendronat veckotablett 70 mg skall tas på fastande mage med ett stort glas vatten, minst 30 minuter före frukost. Patienten får inte ligga förrän efter frukost. Kalcium ska inte tas i nära anknytning till perorala bisfosfonater, enklast för patienter är därför att ta kalcium och D-vitamin på kvällen.
Risedronat, 35 mg tablett 1 ggr/ vecka
Risedronat är en bisfosfonat som ibland används vid biverkningar av alendronat. Såväl effekt som biverkningsprofil liknar de av alendronat och veckotabletten tas på samma sätt. Behandlingstiden rekommenderas på samma sätt. Man bör dock beakta att retentionstiden i skelettet är något kortare än för alendronat och DXA-mätning bör utföras vartannat år efter utsättning. Man kan för risedronat förvänta sig att behöva återinsätta läkemedlet inom 3-4 år efter utsättning.
Zoledronsyra 5 mg iv infusion 1 ggr/år
Initialt behandlas patienten vanligen under 3 år. Kan förlängas upp till 6 år för patienter med kvarvarande hög frakturrisk (samma kriterier som för förlängd behandling med alendronat dvs mer än en kotkompression eller mätmässig osteoporos i höft).
Zoledronsyra har längst retentionstid i benvävnaden av bisfosfonaterna. Efter utsättning avtar även här effekten och man bör räkna med att återinsätta zoledronsyra senast efter cirka 6 års uppehåll. DXA-mätning vart 3:e år efter utsättning rekommenderas om det påverkar fortsatt handläggning.
Zoledronsyra, intravenös bisfosfonatbehandling. Infusion ges i öppenvård under minst 15 minuter, följt av 10 minuters vila innan patienten kan lämna mottagningen. Då patienten inte får vara dehydrerad ska hen dricka 1-2 glas vatten före och efter infusionen. Intag av paracetamol 1g 2-4 gånger rekommenderas under infusionsdagen, för att minska risken för influensaliknande biverkan.
Denosumab 60 mg subkutan injektion var 6:e månad
Denosumab är en human antikropp riktad mot RANK-ligand och ett alternativ till bisfosfonater vid nedsatt njurfunktion eller där bisfosfonater inte tolererats eller av annan anledning inte bedöms lämpliga. Denosumab minskar hos postmenopausala kvinnor med osteoporos risken för kotfraktur med cirka 70%, för höftfraktur med cirka 40% och övriga frakturer cirka 20% jämfört med placebo (4).
Före första injektionen skall S-Calcium och S-Kreatinin. Enligt FASS skall S-Calcium kontrolleras före varje injektion, men på en del kliniker kontrolleras S-Calcium en gång per år om S-Calcium varit stabilt efter de första injektionerna.
Denosumab skall inte utan noggrant övervägande utsättas utan behandlingen bör fortgå kontinuerligt. Effekten av denosumab avtar snabbt cirka 6 månader efter den senaste injektionen, och bentätheten förväntas cirka 18 månader efter den senaste injektionen ha återgått till den nivå man hade före insättning, även om patienten behandlats i flera år. Detta gör att den frakturreducerande effekten snabbt avtar efter utsättning. Om man trots detta behöver/önskar avsluta behandling med denosumab så bör/skall den efterföljas av en behandlingsperiod med bisfosfonater (förutsatt att patienten tål detta med avseende på njurfunktion).
Behandling med denosumab kan ge förhöjd risk för hypokalcemi. Särskild försiktighet bör iakttas hos patienter med uttalat nedsatt njurfunktion. Kontroll av S-kalcium och PTH skall vid njurinsufficiens alltid göras före första dosen och såväl ett lågt serumkalcium som ett förhöjt PTH kan indikera ökad risk för hypokalcemi. Risken för hypokalcemi är störst vid första injektionen men S-kalcium skall kontrolleras före varje dos denosumab vid njurinsufficiens.
Hos patienter med uttalat nedsatt njurfunktion (GFR<30ml/min) och framför allt vid högt PTH, är risken för hypokalcemi särskilt stor. Då bör injektionen föregås av ökat intag av kalcium under ett par veckors tid, eventuellt aktivt vitamin D samt kontroller av S-kalcium före och tämligen snart efter injektionen (4-7 dagar efter injektion plus 4-7 dagar senare). Före första injektionen bör man vid osäkerhet rådgöra med njurmedicinsk specialist, eller läkare med vana att behandla patienter med uttalat nedsatt njurfunktion med denosumab.
Anabola läkemedel och sekventiell behandling
De anabola läkemedlen teriparatid och romosozumab har i randomiserade studier visats mer effektiva än bisfosfonater för patienter med mycket hög frakturrisk som haft en eller flera kotkompressioner. De ger en större ökning i bentäthet och minskar frakturrisken signifikant jämfört med bisfosfonater. Effekten av de anabola läkemedlen på bentäthet blir bättre om behandlingssekvensen inleds med anabol behandling än om antiresorptiv behandling ges först (5). Därför är det viktigt att de övervägs tidigt för selekterade patienter med mycket hög frakturrisk. För att bibehålla den minskade frakturrisken och den ökade benmassan är det dessutom viktigt att man vid behandlingsslut fortsätter med antiresorptiva läkemedel, s.k. sekventiell behandling vilket är praxis. Benuppbyggande läkemedel är mer kostsamma än antiresorptiva läkemedel.
För patienter med mycket hög frakturrisk och låg benmassa bör behandlingen individualiseras och sekventiell behandling kan övervägas. Det kan till exempel vara patienter med en eller flera kliniska kotkompressioner samt kotkompressioner i samband med kronisk kortisonbehandling. Även till patienter med andra frakturer, mycket hög risk och låg bentäthet kan sekventiell behandling övervägas. Benuppbyggande läkemedel (teriparatid eller romosozumab) bör insättas av specialister väl förtrogna med handläggning av osteoporospatienter.
Sammanfattningsvis kan anabola läkemedel övervägas i första hand vid
- en eller flera kliniska kotkompressioner efter lågenergitrauma
- klinisk kotkompression och pågående kortisonbehandling
- en eller flera andra osteoporosfrakturer, mycket hög frakturrisk (t ex FRAX eller annan riskvärdering) i kombination med låg bentäthet
- uttalat låg bentäthet efter benmetabol specialistutredning
Teriparatid (20 μg daglig subkutan injektion)
Teriparatid är ett fragment av humant parathormon, innehåller den aktiva delen (1-34) och verkar direkt på osteoblasterna.
Behandling med teriparatid medförde en signifikant lägre risk för kotfraktur och klinisk fraktur jämfört med risedronat i en studie av postmenopausala kvinnor med hög frakturrisk och kotkompression (VERO) (6). I VERO-studien randomiserades 1360 kvinnor med en svår eller två måttliga kotkompressioner och låg bentäthet (<-1.5 SD i T-score) till teriparatid eller risedronat under 24 månader. Studien visade betydligt lägre incidens av nya kotfrakturer (56% lägre relativ risk) och 52% lägre risk för klinisk fraktur i teriparatidgruppen oavsett om man var behandlingsnaiv eller hade behandlats med bisfosfonater före studiens start.
Långtidseffekten på bentäthet blir större om teriparatid ges före antiresorptiv behandling (s.k sekventiell behandling) jämfört med att börja med enbart antiresorptiv behandling (3). Teriparatid är bland annat kontraindicerat vid tumörer i skelettet och efter strålbehandling.
Teriparatid ges från 18 till maximalt 24 månader. Viktigt att vid utsättning övergå till antiresorptivt läkemedel för att bibehålla effekten av behandlingen och frakturskyddet, då den anabola effekten avtar snabbt efter avslutad behandling
Teriparatid finns nu tillgängligt även i form av biosimilarer och generika, vilket påverkar prisbilden gynnsamt.
Romosozumab, 210 mg (två subkutana injektioner på 105 mg vardera) en gång per månad
Romosozumab är en humaniserad monoklonal antikropp som hämmar sklerostin och medför ökad benbildning genom att aktivera osteoblaster. Romosozumab hämmar också osteoklaster varvid det sker en minskning av benresorptionen.
Behandling med romosozumab medförde en signifikant lägre risk för fraktur jämfört med alendronat i en studie av postmenopausala kvinnor osteoporos och kotkompression eller höftfraktur (7). I ARCH-studien randomiserades 4093 postmenopausala kvinnor med kotkompression och låg bentäthet till romosozumab eller alendronat i 12 månader, och därefter fick alla deltagare alendronat. Kvinnor som fick romosozumab ökade betydligt mer i bentäthet och hade lägre incidens av nya kotfrakturer och höftfrakturer (50 % lägre relativ risk för kotfraktur och 38% lägre risk för höftfraktur) än kvinnor som enbart fick alendronat. Romosozumab är kontraindicerat hos patienter med tidigare hjärtinfarkt eller stroke.
Romosozumab ges i 12 månader. Viktigt att vid utsättning övergå till antiresorptivt läkemedel för att bibehålla effekten av behandlingen och frakturskyddet, då den anabola effekten avtar snabbt efter avslutad behandling.
Läkemedelsinsättning och behandlingskontroll
Kontrollera följsamhet efter 2-3 månaders behandling med p.o. bisfosfonat (kan med fördel göras per telefon / digitalt).
Om behandlingen föregåtts av DXA-mätning kan bentätheten följas upp beroende på behandlingsplanen, i regel efter 2-3 år men kan t ex utsträckas till 5 år och inför ställningstagande om uppehåll om patienten tolererar behandlingen och har god följsamhet. Hos många patienter, särskilt de allra äldsta och de som startar behandling med densumab tillsvidare behöver man inte rutinmässigt göra någon uppföljande DXA-mätning.
Vid behandling med teriparatid utförs DXA-mätningen lämpligen då behandlingen avslutas, dvs efter 18 eller 24 månader. Denna behandlingskontroll utgör utgångspunkt för inledning av antiresorptivt läkemedel.
Vid behandling med romosozumab utförs DXA-mätning lämpligen då behandlingen avslutas, dvs efter 12 månader. Denna behandlingskontroll utgör utgångspunkt för inledning av antiresorptivt läkemedel.
Om signifikant sjunkande bentäthet eller nytillkommen kotkompression bör följsamheten kontrolleras (vid p.o behandling) och terapibyte övervägas. Eventuella orsaker och ytterligare utredning bör övervägas för att utesluta nytillkommen underliggande sjukdom. Om behandlingen bedöms vara framgångsrik behöver bentätheten inte kontrolleras förrän efter ytterligare ca 3 år eller när behandlingen avslutas.
Läkemedelsbiverkningar
Biverkningar vid antiresorptiv behandling
Mag- och tarmbesvär rapporteras inte sällan vid peroral bisfosfonatbehandling, något oftare i samband med alendronat. En mer ovanlig biverkan av bisfosfonat är led- och muskelsmärta. Vid intravenös behandling med zoledronsyra är det vanligt med feber, muskel-, led- och huvudvärk samt influensaliknande symptom under 1-2 dygn efter infusionen. Risken för biverkningar avtar med infusionstillfälle (45% vid 1:a dosen till 10% vid 3:e dosen) och om profylax med analgetika används (19% till 10%, 1:a respektive 3:e dos).
I registreringsstudien för denosumab (FREEDOM), rapporterades en ökad risk för hudinfektion som ledde till sjukhusinläggning (0,4% vs. 0,1% i placebogruppen), samt för eksem. Dessa biverkningar har inte rapporterats från de andra studierna. Risk för hypokalcemi skall beaktas för vissa grupper, se ovan.
Biverkningar vid anabol behandling
Generellt, vid behandling med teriparatid är eventuella biverkningarna milda och övergående. Vanliga biverkningar inkluderar illamående, yrsel (3-9%), ortostatisk hypotension, benkramper (ca 3%) och hyperkalcemi, vanligtvis mild. Observera att om man kontrollerar S-Calcium, så bör patienten provtagningsdagen ta teriparatid och eventuell calciumtablett efter provtagningen. Osteosarkom har observerats hos råttor, men ingen sådan ökad risk har påvisats hos människor som behandlats med teriparatid. Teriparatid är kontraindicerat hos patienter med skelettmetastasering, osteosarkom eller om skelettet strålbehandlats.
Vid behandling med romosozumab är eventuella biverkningarna milda och övergående. En vanlig biverkan är hudreaktion vid injektionsstället (ca 5%). I ARCH-studien (romosozumab vs. alendronat), sågs en överrisk av allvarliga kardiovaskulära händelser (2.0% vs. 1.1%). Ingen sådan överrisk observerades däremot inte i den större placebokontrollerade FRAME-studien (8). Romosozumab är kontraindicerat vid tidigare hjärtinfarkt eller stroke.
Sällsynta biverkningar
Bisfosfonatbehandling medför ökad risk för osteonekros i käken (ONJ). Incidensen hos patienter med skelettmetastasering (som ges mycket högre doser) beräknas till 1-15%. Hos osteoporospatienter är incidensen nära den för allmänna befolkningen (0,001 till 0,01% jämfört med <0,001%) (9). Evidens talar för att risken för för ONJ vid behandling med denosumab liknar den vid bisfosfonater.
Risken för atypisk subtrokantär femurfraktur är förhöjd och ökar med behandlingsduration (3.2-50 fall per 100 000 personår). Befintlig evidens talar för att risken för atypisk femurfraktur med denosumab liknar den för bisfosfonater.
Risk-nyttosambandet har bland annat beskrivits utifrån följande exempel: 5 års behandling med bisfosfonater hos 10 000 patienter resulterar i att 286 höftfrakturer, 859 kliniska frakturer undviks på bekostnad av 8 atypiska femurfrakturer (10-11).
Läkemedelsbehandling hos äldre och efter höftfraktur

Patienter som är äldre bör handläggas på samma sätt som yngre patienter. Utredningsgången anpassas efter patientens hälsostatus och förväntad överlevnad bör vägas in i utrednings- och behandlingsbeslut in hos de biologiskt allra äldsta. Då bentäthetsmätning kan vara svårt att få till stånd hos äldre och sköra patienter med kot- eller höftfrakturer, kan läkemedelsbehandling i lämpliga fall ges utan föregående mätning.
Tack vara långvarig effekt och god följsamhet är zoledronsyra speciellt lämpligt till denna grupp. Vid nedsatt njurfunktion rekommenderas denosumab, och då som tillsvidarebehandling.
Tillgänglig evidens talar för att äldre har lika stor nytta i form av minskad risk för fraktur av osteoporosläkemedel som yngre patienter. Lägre NNT (numbers needed to treat) med osteoporosläkemedel ses dock hos äldre pga. deras högre absoluta risk.
Innan insättande bör man utreda och vid behov inleda behandling för att korrigera eventuell hypokalcemi och vitamin D-brist.
Behandling efter en höftfraktur
I samband med höftfraktur bör behandling med osteoporosläkemedel ges om det inte finns kontraindikationer och behandlingen betraktas som adjuvantterapi. Behandlingsvalet styrs av patientens allmäntillstånd och där kan även ålder vara en faktor. Patienter under 50 år med höftfraktur bör bedömas av specialist då underliggande sjukdomar är vanliga. Hos de äldsta och ofta sköra är injektions- eller infusionsbehandling att föredra och ställningstagandet bör ske i direkt anslutning till vårdtillfället. Beslutet är beroende av hur vården är ordnad och vilka tidsramar och möjligheter som finns. Det är en fördel om första dosen kan administreras i samband med vårdtillfället. Vid korta vårdtider, kan därmed denosumab vara lämpligt läkemedel för de äldsta och sköraste patienterna. Tidsaspekten är viktig hos dessa patienter eftersom risken för nya frakturer är mycket hög redan under de två första åren efter fraktur. Insättande av behandling bör därför ha skett inom fyra månader.
Denosumab har en mer gynnsam biverkningsprofil jämfört med zoledronsyra i nära anslutning till operation, eftersom man undkommer eventuella influensaliknande reaktioner relaterade till zoledronsyrainfusionen, vilka kan leda till förlängd vårdtid. Viktigt att man säkerställer uppföljning inom 6 månader för ställningstagande till fortsatt behandling med denosumab eller om det är lämpligt med byte till zoledronsyra. För lite yngre personer med höftfraktur är zoledronsyra ett förstahands alternativ om man organisatoriskt säkerställer att dosen kan ges vid uppföljning i när anslutning till frakturtillfället.
Referenser
- Black DM, Delmas PD, Eastell R, Reid IR, Boonen S, Cauley JA, et al. Once-yearly zoledronic acid for treatment of postmenopausal osteoporosis. N Engl J Med. 2007;356(18):1809-22.
- Black DM, Thompson DE, Bauer DC, Ensrud K, Musliner T, Hochberg MC, et al. Fracture risk reduction with alendronate in women with osteoporosis: the Fracture Intervention Trial. FIT Research Group. J Clin Endocrinol Metab. 2000;85(11):4118-24.
- Lorentzon M. Treating osteoporosis to prevent fractures: current concepts and future developments. J Intern Med. 2019;285(4):381-94.
- Cummings SR, San Martin J, McClung MR, Siris ES, Eastell R, Reid IR, et al. Denosumab for prevention of fractures in postmenopausal women with osteoporosis. N Engl J Med. 2009;361(8):756-65.
- Langdahl B. Treatment of postmenopausal osteoporosis with bone-forming and antiresorptive treatments: Combined and sequential approaches. Bone. 2020;139:115516.
- Kendler DL, Marin F, Zerbini CAF, Russo LA, Greenspan SL, Zikan V, et al. Effects of teriparatide and risedronate on new fractures in post-menopausal women with severe osteoporosis (VERO): a multicentre, double-blind, double-dummy, randomised controlled trial. Lancet. 2018;391(10117):230-40.
- Saag KG, Petersen J, Brandi ML, Karaplis AC, Lorentzon M, Thomas T, et al. Romosozumab or Alendronate for Fracture Prevention in Women with Osteoporosis. N Engl J Med. 2017;377(15):1417-27.
- Cosman F, Crittenden DB, Adachi JD, Binkley N, Czerwinski E, Ferrari S, et al. Romosozumab Treatment in Postmenopausal Women with Osteoporosis. N Engl J Med. 2016;375(16):1532-43.
- Khosla S, Burr D, Cauley J, Dempster DW, Ebeling PR, Felsenberg D, et al. Bisphosphonate-associated osteonecrosis of the jaw: report of a task force of the American Society for Bone and Mineral Research. J Bone Miner Res. 2007;22(10):1479-91.
- Black DM, Geiger EJ, Eastell R, Vittinghoff E, Li BH, Ryan DS, et al. Atypical Femur Fracture Risk versus Fragility Fracture Prevention with Bisphosphonates. N Engl J Med. 2020;383(8):743-53.
- Gedmintas L, Solomon DH, Kim SC. Bisphosphonates and risk of subtrochanteric, femoral shaft, and atypical femur fracture: a systematic review and meta-analysis. J Bone Miner Res. 2013;28(8):1729-37.
PM – parenterala läkemedel
Träning och andra livsstilsåtgärder
Fysisk träning
Träningsrekommendationerna skiljer sig mellan patienter som endast har diagnosen osteoporos men inga frakurer och de som har en fraktur nyligen eller tidigare. Typ av fraktur och lokalisation spelar då också roll. Till de som inte haft någon fraktur kan belastande träning av skelettet rekommenderas. För de som haft en fraktur, måste träningen anpassas till tiden från fraktur och typ av fraktur och skiljer sig mellan de som haft armfraktur och de patienter som haft kot-, höft- eller bäcken fraktur; här ligger fokus på muskel och funktionsträning. Alla behöver kontinuerlig specifik balansträning för att undvika fall.
Mekanisk belastning är viktig för att förhindra benförlust och eventuellt öka bentätheten. Belastande träning som patienterna trivs med rekommenderas 2-3 ggr/vecka med successivt ökad träningsgrad kombinerat med 30 minuter dagliga raska promenader/jogging. Därigenom kan också muskler stärkas och koordination förbättras. Träning ska anpassas till ålder och funktionsnivå.
Träning vid kotfraktur
Fokus ska ligga på träning av ryggmuskelsträckare samt träning av bålstabillitet. Hos patienter med osteoporos är ryggmuskelsträckare betydligt svagare än hos friska kvinnor. Har patienten dessutom kyfos är ryggmuskelsträckare än svagare, och ju fler kotkompressioner, desto svagare ryggmuskelsträckare. Patienterna hänvisas till sjukgymnast/fysioterapeut med specifik kunskap om ryggmuskelträning och bål-stabiliserande träning vid osteoporos (framåtböjning som vid tex sit ups och vridningar är kontraindicerade). Träning kan ske i grupp med individuell belastning 2 ggr/vecka à 45 min och kombineras med hemträningsprogram. Andningsförmåga och välbefinnande förväntas öka, medan kyfos och smärta kan minska. Ryggmuskelkraften och bålstabiliteten ökar och åldersassocierad sarkopeni motverkas. Ett antal mindre randomiserad kontrollerade studier talar för positiv effekt på muskelstyrka, kyfos, längd, andning, balans, smärta och välbefinnande med positiva resultat finns. Avseende muskulär styrketräning summeras 121 randomiserade studier som visar att styrketräning hos äldre har stor effekt på muskelstyrkan med en ökning upp till 200 % (1).
Träning vid höftfraktur
Det primära är att patienterna återfår normalt gång och rörelsemönster. Utöver gångträning rekommenderas generell muskelstärkande och muskelfunktionsökande träning. Mobilisering ska starta så snart som möjligt, helst inom 48 timmar postoperativt. Specifik träning, initierad av sjuk-gymnast/fysioterapeut, bör innehålla både viktbärande och icke viktbärande övningar. Träningen ska ske dagligen med individuell belastning och hög intensitet och innehålla muskelspecifika och funktionella övningar som ökar benmuskelstyrka och förbättrar balans. Härmed motverkas försämrad funktionsförmåga.Rehabilitering i öppenvården utformas efter patientens förutsättningar. Hemträning med fysioterapeut har visat sig förbättra gång och fysisk förmåga jämfört med standard vård. Studier av träningsintervention utöver sedvanlig rehabilitering och funnit förbättrad fysisk förmåga (2).
Adekvat rehabilitering både i det korta och längre perspektivet är väsentlig oavsett boendeform och kompetent personal behöver finnas där patienterna vistas så att fler patient återfår sin gångförmåga.
Fallprevention
Teamarbete krävs för effektiv fallprevention med fokus på riskfaktorer hos individen och i dess omgivning. Fallriskbedömning ska ske på individuell basis avseende syn- och reaktionsförmåga, proprioception, muskelstyrka och balansförmåga. Rädsla för att falla är starkt kopplat till förekomst av nya fall – och mycket enkelt att fråga om. Likaså om man haft ett eller flera fall under senaste året.Balans-, koordinations- och styrketräning, anpassade gånghjälpmedel, halkskydd, bostadsanpassning och översyn av utemiljö kan minska fallrisk (3). Genomgång av läkemedelsbehandling och vid behov dosminskning eller utsättning av läkemedel som ökar fallrisken, så som sedativa, sömnmedel, centralt verkande smärtstillande, hypertoniläkemedel m.fl. Vitamin D brist bör undvikas eftersom det kan öka fallrisken.
Andra levnadsvanor
Kost och nutrition har betydelse för skelettet och utgångspunkten är en balanserad kost som inte utesluter viktiga komponenter. Undervikt/malnutrition är en riskfaktor för låg bentäthet och fraktur. Riskgrupper är patienter med BMI under 19, malnutrierade, fetmaopererade, veganer, anorexipatienter och personer med extremkost. Viktökning ger ökad bentäthet. Överväg att remittera patienter med lågt BMI till dietist. Näringstillskott rekommenderas vid kakexi hos de äldsta. Viktminskning ska undvikas för att få bra effekt av medicinsk osteoporosbehandling.Kost innehållande t.ex. fet fisk och berikade mjölkprodukter samt en stunds daglig solexponering, under sommarhalvåret, ökar D vitaminnivåerna och rekommenderas därför.
Rökning påverkar bentätheten negativt och ökar frakturrisken; ju längre tid som rökare desto större risk. Rökstopp minskar risken successivt över tid. Överväg remiss för hjälp till rökstopp.
Alkohol ökar risk för fraktur genom direkt effekt på skelettet, men också genom benägenhet för fallskador. Alkoholanamnes efterfrågas och överkonsumtion ska uppmärksammas och riktad vård erbjudas. Med riskbruk avses; mer än 9 standardglas per vecka för kvinnor och mer än 14 standardglas i vecka för män. Även andra beroende kan vara av betydelse såsom överkonsumtion av psykofarmaka eller droger.
Referenser
- Liu CJ, Latham NK. Progressive resistance strength training for improving physical function in older adults. Cochrane Database Syst Rev. 2009;2009(3):Cd002759.
- Lee SY, Jung SH, Lee SU, Ha YC, Lim JY. Effect of Balance Training After Hip Fracture Surgery: A Systematic Review and Meta-analysis of Randomized Controlled Studies. J Gerontol A Biol Sci Med Sci. 2019;74(10):1679-85.
- Sherrington C, Fairhall NJ, Wallbank GK, Tiedemann A, Michaleff ZA, Howard K, et al. Exercise for preventing falls in older people living in the community. Cochrane Database Syst Rev. 2019;1(1):Cd012424.
Osteoporos hos män
Osteoporos med fraktur har betraktats som en typisk kvinnlig sjukdom. När diagnosen definierades 1994 av WHO omfattade diagnoskriterierna enbart vuxna kvinnor och inte män eller barn. Däremot har FRAX utvecklats både för män och kvinnor även om skattningar för frakturrisk är osäkrare för män. Bentäthet i höft predikterar höftfraktur lika bra hos män som hos kvinnor. Unga män och pojkar har högre risk för fraktur jämfört med unga kvinnor och flickor sannolikt beroende på en högre förekomst av trauma. Efter menopausålder har kvinnor en klart högre risk för/förekomst av osteoporos och osteoporosrelaterade frakturer. Män har större och grövre ben som ger högre hållfasthet och leder till färre frakturer än hos kvinnor. I åldrar över 80 år är könsskillnaderna avseende risken för höftfraktur mindre.
Det har tidigare ansetts att sekundär osteoporos är vanligare hos män än hos kvinnor pga. levnadsvanor som rökning och högt alkoholintag. Andelen män i ålder 60-70 år med hypogonadism är bara 10%, medan alla kvinnor vid denna ålder är i menopaus. Androgendeprivationsterapi (ADT) vid prostatacancer leder till låga nivåer av östrogen och testosteron, vilket ökar risken för osteoporos och frakturer. En svensk registerstudie har visat 40 % ökad risk för osteoporosfraktur och höftfraktur vid ADT behandling (1).
Män med lågenergifrakturer underbehandlas i ännu högre grad än kvinnor . Den absoluta majoriteten av randomiserade läkemedelsstudier mot osteoporosfrakturer har endast inkluderat kvinnor. I en studie av män med låg benmassa har zoledronsyra visats förebygga kotfrakturer. I en annan studie av män som behandlades med antiandrogener mot prostatacancer sågs en minskning av nya kotfrakturer vid behandling med denosumab.
Läkemedelsbehandling för män i samma dos som används hos kvinnor är godkänd av Läkemedelsverket, då det visats att läkemedlen ökat benmassan på ett liknande sätt som hos kvinnor. Peroral veckodos bisfosfonat, zoledronsyra i årlig infusion, subkutan injektion av denosumab samt teriparatid är godkända behandlingar för manlig osteoporos. Vid manlig sekundär osteoporos vid kortisonbehandling är behandling med bisfosfonat eller teriparatid godkänd.
Referenser:
- Wallander M, Axelsson KF, Lundh D, Lorentzon M. Patients with prostate cancer and androgen deprivation therapy have increased risk of fractures-a study from the fractures and fall injuries in the elderly cohort (FRAILCO). Osteoporos Int. 2019;30(1):115-25
Låg bentäthet hos barn och unga
Barn och unga vuxna med nedsatt bentäthet bör utredas av och ha kontakt med center/klinik med stor erfarenhet av nedan specificerade ovanliga tillstånd. Barn bör utredas av barnläkare.
Benskörhet förekommer hos barn och ungdomar men är sällsynt såväl i primär som i sekundär form.
Indikation för bentäthetsmätning av barn och unga:
- Återkommande lågenergifrakturer
- Kotkompressioner
- Hereditet
- Kliniska tecken på benmetabol sjukdom (blå sklerae, sköra tänder, hörselnedsättning, överrörlighet)
- Amenorré
- Muskelsjukdom
- Hög grad av immobilisering
- Långvarig steroidbehandling
Hos barn, män < 50 år och premenopausala kvinnor används inte begreppet ”osteoporos” utan istället används ”låg bentäthet för åldern”.
Låg bentäthet för åldern föreligger vid Z –score < – 2 mätt med DXA. Mätning av barn (växande individer) bör utföras på helkropp (minus huvud) och ländrygg.
Orsaker till nedsatt bentäthet hos barn och unga
Primär benmetabol sjukdom
- Osteogenesis imperfecta (OI) (ärftlig, mycket heterogen sjukdom som oftast orsakas av kollagen typ 1 mutationer)
- Andra ovanliga genetiska sjukdomar i kalk- och fosfatomsättningen (x-kromosombunden hypofosfatemisk rakit, skelettdysplasier)
- Juvenil osteoporos (bakomliggande sjukdom är utesluten)
- Idiopatisk osteoporos (hos unga vuxna, annan sjukdom är utesluten)
Andra orsaker till nedsatt bentäthet
Barn och unga vuxna kan liksom vuxna drabbas av osteoporos vid många olika sjukdomar sekundärt till imobilisering, malnutrition, skelettpåverkande läkemedel/behandlingar, eller mer specifika rubbningar i benmetabolismen, t.ex. systemiska inflammatoriska sjukdomar, malabsorption, tyreoideasjukdom, muskeldystrofier, anorexi, njursvikt och läkemedel, organ/benmärgstransplantation, cytostatikabehandling (se även avsnitt sekundär osteoporos).
Några av dessa sjukdomar, behandlingar och läkemedel leder till amenorré/hypogonadism; primär och sekundär amenorré hos flickor respektive hypogonadism hos pojkar kan också förekomma vid, tex anorexi, hypotalamisk påverkan, hypofystumörer (som t.ex. prolaktinom), eller extensiv fysisk träning; hos flickor vid Turners syndrom och prematur ovariell insufficiens; eller hos pojkar vid Kallmans syndrom. Dessa tillstånd leder pga. könshormonbristen till nedsatt bentäthet.
Diagnos ställs genom samlad klinisk bedömning, laborativ utredning och i ökad utsträckning genetisk analys. Barnmisshandel är en differentialdiagnos vid multipla frakturer hos spädbarn och små barn.
Behandling av låg bentäthet hos barn och unga vuxna
- Kontakt med center/klinik med stor erfarenhet av benmetabola sjukdomar hos barn
- Behandla bakomliggande sjukdomar
- Viktbärande fysisk aktivitet, om möjligt i form av lek med hopp
- Optimera nutrition (bl. a. vitamin D, kalcium)
- Viktuppgång vid anorexi
- Östrogen/progesteron vid ovariell svikt, testosteron vid gonadsvikt
- Vid behov, benspecifik behandling
Organisation för sekundärprevention – frakturkedjor
I Sverige råder stor underbehandling av patienter med tidigare osteoporosrelaterade frakturer enligt Socialstyrelsens Öppna Jämförelser. En systematisk riskvärdering, utredning och vid behov behandling av dessa patienter är ett effektivt och kostnads- besparande sekundärpreventivt arbetssätt. Det ökar adekvat läkemedelsbehandling och ökar andra åtgärder för minska risken för fraktur, där fallprevention är särskilt viktigt med stigande ålder. En strukturerad frakturkedja bör organiseras vid varje sjukhus som handlägger frakturpatienter.
Frakturkedja som åtgärd får högsta prioritet i Socialstyrelsens senaste riktlinjer om osteoporos (2020). Läkemedelsverket (2020) betonar på samma sätt att alla postmenopausala kvinnor samt män över 50 år som drabbas av en fraktur ska utredas för osteoporos och benspecifik läkemedelsbehandling ska alltid övervägas.
Statens kommuner och regioner (SKR) har initierat utarbetande av ett personcentrerat och standardiserat vårdförlopp (PSV Osteoporos) för att säkerställa att alla frakturpatienter, 50 år och äldre utreds och v.b. erbjuds fall- och frakturförebyggande åtgärder. Implementering påbörjas under 2021 inom ramen för Kunskapsstyrning. Frakturkedjan är ett sätt att omgående hitta patienter men nyligen genomgången fraktur medan andra strategier behövs för övriga personer med risk för osteoporos. Frakturkedjan ska också säkra att alla delar i vårdförloppet länkar i varann.
Frakturkoordinatorerna, ibland kallade osteoporoskoordinatorer, har en central roll i frakturkedjan för identifieringen av patienter med osteoporosrelaterade frakturer, vanligen där de handläggs i det akuta skedet. Koordinatorna riskvärderar patienterna med hjälp av FRAX, andra kliniska riskfaktorer samt uppskattar fallbenägenhet. Om kriterier för vidare utredning finns kan DXA-mätning föreslås i samråd med patienten. Resultat av DXA-mätning samt frakturrisk utvärderas av medicinskt ansvarig. Förslag avseende farmakologisk och/eller annan behandling inkl. fallpreventiva åtgärder förmedlas till patientens allmänläkare som tillsammans med patienten avgör vilka åtgärder som ska initieras.
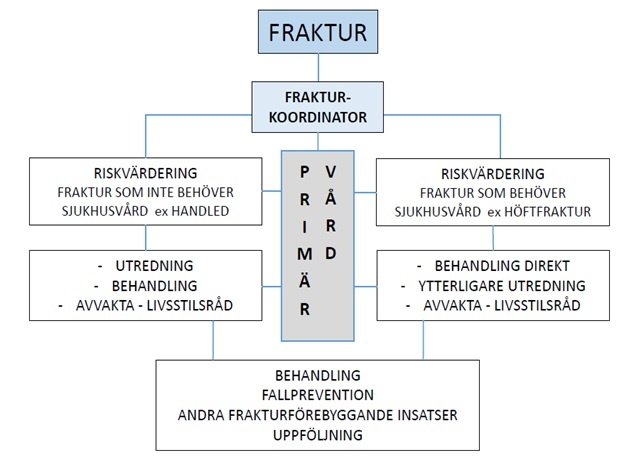
Majoriteten av patienterna handläggs därmed i primärvården. Övergången mellan sluten och öppenvård/primärvård kan variera beroende på lokala förutsättningar.
Därmed är samarbetet mellan de olika vårdgivarna avgörande – att optimera frakturprevention är ett multidisciplinärt och interprofessionellt teamarbete i alla delar.
En mindre andel patienter handläggs på specialiserad osteoporosmottagning, företrädesvis patienter där sekventiell behandling kan bli aktuell (patienter med mycket hög frakturrisk, som vid uttalad osteoporos eller multipla frakturer/kotkompressioner), eller patienter med andra benmetabola sjukdomar. Parenteral behandling (zoledronsyra och denosumab) ska kunna ges även i primärvård.
Läs mer om SKR vårdförlopp Osteoporos här!
Rekommendationer för diagnossättning
Bakgrund till rekommendationerna
Att i svenska journalsystem ställa diagnosen osteoporos på ett standardiserat sätt är viktigt för att kunna kvalitetssäkra vård och även genomföra registerstudier inom denna patientgrupp. Diagnosen osteoporos, som den används än idag fastslogs av WHO 1994 och definierar osteoporos respektive osteopeni enbart utifrån bentäthetsmätning utförd med DXA i ländrygg eller höft (och ibland radius) [1]. Att enbart basera osteoporosdiagnosen på bentäthetsmätning kan dock vara missvisande då patienter med osteopeni kan ha en sammantaget mycket hög frakturrisk och många av de allra äldsta patienter får behandling med osteoporosläkemedel även utan genomgången bentäthetsmätning. Ibland kan även bentäthetsmätningen vara missvisande på grund av skelettpålagringar och andra åldersförändringar som ger falska värden. En amerikansk expertgrupp publicerade 2014 riktlinjer kring diagnossättning av osteoporos. Experterna var utsedda av Nationella osteoporosföreningen (NOF) samt även amerikanska osteoporosföreningen (ASBMR) och även amerikanska ortopediförbundet (AAOS) [2]. Mot bakgrund av detta och med anpassning till svenska förhållanden har nu Svenska Osteoporossällskapet beslutat om följande rekommendationer.
Rekommendation gäller för vårdkontakter där man kan göra en helhetsbedömning av bentäthet och frakturrisk (såsom vid läkarbesök/telefonkontakt eller klinisk tolkning av DXA).
De övergripande diagnoserna rekommenderas för både män och kvinnor i primärvård och sjukhusvård. För de som vill kan man även välja en mer specificerad diagnos enligt nedan, huvudsaken är att M8… registreras i patientjournalen.
Övergripande diagnoser som kan användas för både män och kvinnor
M80.9 (Osteoporos ospec. med fraktur)
- Osteoporos via DXA samt lågenergifraktur.
- Genomgången höftfraktur pga. lågenergivåld (oavsett DXA)
- Osteopeni via DXA samt en eller flera lågenergifrakturer med indikation för osteoporosläkemedel (t.ex. kotkompression eller andra frakturer samt hög frakturrisk).
- En eller flera lågenergifrakturer där osteoporos bedöms vara den mest sannolika bakomliggande orsaken men där DXA inte bedöms vara genomförbart (t. ex hög ålder, multisjuklighet).
M81.9 (Osteoporos ospec. utan fraktur)
- Osteoporos via DXA utan fraktur.
- Osteopeni via DXA utan fraktur fast med indikation för osteoporosläkemedel.
- Patienter utan fraktur men med indikation för osteoporosläkemedel men där DXA inte bedömdes vara genomförbart.
M85.9 (Andra rubbningar i bentäthet och benstruktur, ospec)
- Osteopeni med eller utan lågenergifrakturer, utan indikation för osteoporosläkemedel.
- Barn (< 18 år) med låg bentäthet.
Mer specificerade diagnoser
M80.0 (Osteoporos efter menopausen med fraktur)
- Som M80.9 men enbart för postmenopausala kvinnor
M81.0 (Osteoporos efter menopausen utan fraktur)
- Som M81.9 men enbart för postmenopausala kvinnor
M80.4 (Läkemedelsutlöst osteoporos med fraktur)
- Som M80.9 men där läkemedel bedöms vara den huvudsakliga bakomliggande orsaken (t .ex kortison).
M81.4 (Läkemedelsutlöst osteoporos utan fraktur)
- Som M81.9 men där läkemedel bedöms vara den huvudsakliga bakomliggande orsaken (t. ex kortison).
M80.5 (Idiopatisk osteoporos med fraktur)
- Män och kvinnor med låg benmassa samt tidigare lågenergifraktur där ingen bakomliggande orsak kan identifieras (Oftast yngre män och kvinnor, används framförallt på specialistmottagningar).
M81.5 (Idiopatisk osteoporos)
- Män och kvinnor med låg benmassa utan fraktur där ingen bakomliggande orsak kan identifieras. (Oftast yngre män och kvinnor, används framförallt på specialistmottagningar).
Referenser
- Osteoporosis prevention, diagnosis, and therapy. NIH Consens Statement, 2000. 17(1): p. 1-45.
- Siris, E.S., et al., The clinical diagnosis of osteoporosis: a position statement from the National Bone Health Alliance Working Group. Osteoporos Int, 2014. 25(5): p. 1439-43.
Bakgrund till rekommendationerna
Att i svenska journalsystem ställa diagnosen osteoporos på ett standardiserat sätt är viktigt för att kunna kvalitetssäkra vård och även genomföra registerstudier inom denna patientgrupp. Diagnosen osteoporos, som den används än idag fastslogs av WHO 1994 och definierar osteoporos respektive osteopeni enbart utifrån bentäthetsmätning utförd med DXA i ländrygg eller höft (och ibland radius) [1]. Att enbart basera osteoporosdiagnosen på bentäthetsmätning kan dock vara missvisande då patienter med osteopeni kan ha en sammantaget mycket hög frakturrisk och många av de allra äldsta patienter får behandling med osteoporosläkemedel även utan genomgången bentäthetsmätning. Ibland kan även bentäthetsmätningen vara missvisande på grund av skelettpålagringar och andra åldersförändringar som ger falska värden. En amerikansk expertgrupp publicerade 2014 riktlinjer kring diagnossättning av osteoporos. Experterna var utsedda av Nationella osteoporosföreningen (NOF) samt även amerikanska osteoporosföreningen (ASBMR) och även amerikanska ortopediförbundet (AAOS) [2]. Mot bakgrund av detta och med anpassning till svenska förhållanden har nu Svenska Osteoporossällskapet beslutat om följande rekommendationer.
Rekommendation gäller för vårdkontakter där man kan göra en helhetsbedömning av bentäthet och frakturrisk (såsom vid läkarbesök/telefonkontakt eller klinisk tolkning av DXA).
De övergripande diagnoserna rekommenderas för både män och kvinnor i primärvård och sjukhusvård. För de som vill kan man även välja en mer specificerad diagnos enligt nedan, huvudsaken är att M8… registreras i patientjournalen.
Senast ändrad: 26 oktober 2022